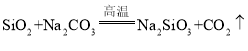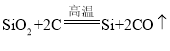题目内容
【题目】硫酸在工农业生产中应用都非常广泛,在工业上可利用黄铁矿(主要成分是FeS2)煅烧的产物冶炼铁和生产硫酸,如图是制取工艺流程。下列说法不正确的是

A.图中过程③生成X为SO3
B.过程②属于工业炼铁,设备为高炉
C.FeS2中硫元素的化合价为一2价
D.工业生产的废气SO2可用熟石灰来吸收
【答案】C
【解析】
A、二氧化硫可与氧气反应生成三氧化硫,故X为SO3,不符合题意;
B、过程②是将铁矿石冶炼成铁,属于工业炼铁,工业炼铁的设备为高炉,通常在高温下,用高炉内反应生成的一氧化碳把铁从铁矿石里还原出来,不符合题意;
C、二硫化亚铁中铁元素的化合价通常为+2价,设硫元素的化合价为x,根据化合物中,正、负化合价的代数和为零,2+2x=0,x=-1,符合题意;
D、氢氧化钙可与二氧化硫反应生成亚硫酸钙,工业生产的废气二氧化硫可用熟石灰来吸收,不符合题意。
故选C。

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目