��Ŀ����
����Ŀ��ij��˾�������Ĵ����Ʒ�о����ֻ�����Ȼ������ʡ�Ϊ�ⶨ��Ʒ��̼���Ƶ�����������20��ʱ����ȡ�ò�Ʒ��Ʒ26��5g�����뵽ʢ��һ������ϡ������ձ��У�̼������ϡ����ǡ����ȫ��Ӧ��������ȫ�ݳ����õ�������NaCl��Һ����Ӧ�����þ�����������ձ��ڻ�����������m���뷴Ӧʱ�䣨t����ϵ����ͼ��ʾ��
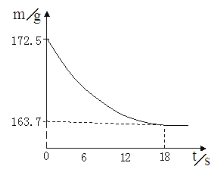
��1������CO2��������
��2����Ӧ��������Һ��NaCl������������
���𰸡� (1)8��8g;(2)16��9%
��������
�����������1�����ɶ�����̼������Ϊ172��5g��163��7 g = 8��8 g
��2���裺��Ʒ��̼���Ƶ�����Ϊx ���������ᷴӦ������NaCl����Ϊy��
Na2CO3 + 2HCl��2NaCl + CO2 �� + H2O
106 117 44
x y 8��8g
106��44=x:8��8g 117��44= y:8��8g
x=106��8��8g/44= 21��2g
y=117��8��8g/44= 23��4g
��Ӧ��������Һ��NaCl����������Ϊ
23��4g��(26��5g��21��2g)��163��7g��100%=16��9%
�𣺣�1�����ɶ�����̼������8��8g��
��2����Ӧ��������Һ��NaCl����������Ϊ16��9%��

��ϰ��ϵ�д�
�����Ŀ


