题目内容
【题目】根据下列各种粒子结构示意图,回答问题:

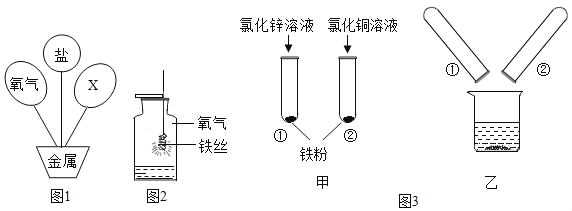
(1)若图A是原子结构示意图,则n=_____。
(2)微粒B、C、D中,属于阴离子的是_____(填编号),对应单质化学性质最稳定的是_____(填化学式)。
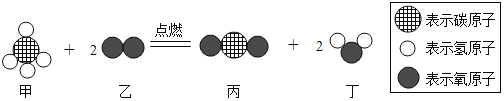
(3)氨的催化氧化是工业上一个重要的反应,该反应前后分子种类的变化微观示意图如图所示,据图回答问题:

①该反应中属于化合物的有_____(写化学式);
②写出该反应的化学方程式_____。
【答案】7 B Ne NH3、NO、H2O 
【解析】
(1)在原子中质子数等于电子数,若图 A 是原子结构示意图,则 n=35﹣2﹣8﹣18=7。
(2)在B中质子数等于9,而电子数等于10,属于阴离子,故阴离子填:B;Ne的最外层电子数是8,达到了稳定结构,对应单质化学性质最稳定,故填:Ne。
(3)①由微粒的构成可知,甲、丙、丁的分子是由不同种的原子构成的,属于化合物,化学式分别是:NH3、NO、H2O;②由变化微观示意图可知,氨的催化氧化反应生成了一氧化氮和水,化学方程式是:4NH3+5O2 4NO+6H2。
4NO+6H2。

 优翼小帮手同步口算系列答案
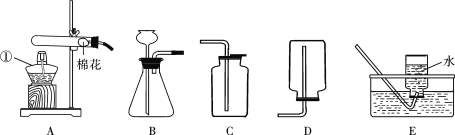
优翼小帮手同步口算系列答案【题目】某研究性学习小组利用如图装置探究温度对CO还原Fe2O3的影响(固定装置略).
查阅资料:CO2+Zn![]() CO+ZnO;FeCl3溶液遇KSCN溶液变红.
CO+ZnO;FeCl3溶液遇KSCN溶液变红.
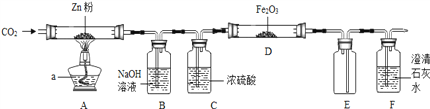
请回答下列问题:
将研究小组分为两组,按如图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D进行加热,其产物均为黑色粉末(纯净物).两组分别用产物进行以下实验:
步骤 | 操作 | 甲组现象 | 乙组现象 |
1 | 取黑色粉末加入盐酸 | 溶解,无气泡,溶液呈浅黄绿色(含两种金属离子) | 溶解,有气泡,溶液呈浅绿色 |
2 | 取步骤1所得溶液,滴加KSCN溶液 | 变红 | 无现象 |
(1)则乙组装置D玻璃管中反应的化学方程式是_________________________________,甲组得到的黑色粉末是______.
(2)从安全考虑,本实验应在装置_____和______之间再添加装置E防止倒吸.(填字母编号)
(3)该对比实验结果表明CO的还原能力随温度的升高而________(填“增强”或“减弱”).
【题目】在一次聚餐中,同学们对燃料“固体酒精”产生了兴趣,于是对该固体酒精的成分进行探究。
(查阅资料)(1)固体酒精由酒精、氯化钙和氢氧化钠按一定质量比例混制成。
(2)氯化钙溶液呈中性,碳酸钠溶液呈碱性。
(提出问题)(1)酒精中是否含有碳元素?
(2)该固体酒精中的氢氧化钠是否变质?
(实验探究)(1)按如图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论,此结论_____(填“合理”或“不合理”)
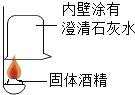
(2)取少量该固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,取沉淀于试管中加稀盐酸,有气泡产生,该气体是_____。
(实验结论)分析实验并结合资料得出氢氧化钠已变质。
(拓展实验)为进一步确定氢氧化钠的变质程度,小北同学做了以下实验:
实验方案 | 实验现象 | 实验结论 |
取烧杯中上层清液于试管中,加入几滴酚酞溶液 | 溶液变红 | 清液中有氢氧化钠 |
另取烧杯中上层清液于试管中,加入澄清石灰水溶液 | 产生_____ | 清液中有碳酸钠 |
(1)有同学认为小北的实验不能证明清液中一定有氢氧化钠,理由是_____。
(2)该同学另取烧杯中上层清液,加入足量的氯化钙溶液充分反应,有白色沉淀生成,反应后滴加酚酞溶液,溶液变红,加入足量氯化钙溶液的目的是_____,写出生成沉淀的化学方程式:_____。
(3)实验结论:固体酒精中氢氧化钠的变质程度是_____(填“完全变质”或者“部分变质”)