题目内容
【题目】小明用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,然后再用废液测定一瓶未知浓度的Na2CO3溶液的溶质质量分数,他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示。
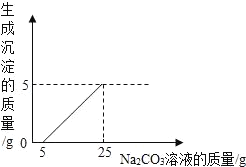
(1)横坐标上0~5这一段所表示的意义是_____。
(2)计算Na2CO3溶液中溶质的质量分数_____。(计算结果精确到0.1%)
【答案】与盐酸反应的碳酸钠溶液的质量 26.5%
【解析】
(1)开始时没有发现沉淀生成,说明Na2CO3溶液没有和CaCl2反应,说明废液中还有没有反应完的稀盐酸,则前5g是与盐酸发生反应的碳酸钠溶液的质量,故填与盐酸反应的碳酸钠溶液的质量。
(2)解:分析图意可知,与氯化钙溶液反应的Na2CO3溶液的质量为25g﹣5g=20g,生成5g碳酸钙沉淀
设:20gNa2CO3溶液中溶质的质量为x
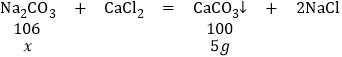
106:100=x:5g
x=5.3g
则该Na2CO3溶液中溶质的质量分数为![]() ×100%=26.5%。
×100%=26.5%。
答:Na2CO3溶液中溶质的质量分数为26.5%。

练习册系列答案
相关题目