题目内容
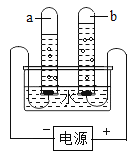
【题目】如下图所示,电解水实验中,通电后电极上出现___________,并汇集到试管上端。正极端的试管内产生的气体能_______________,负极端的试管内产生的气体能______________;则正极端的试管内产生的气体是____________,负极端的试管内产生的气体是____________,说明水是由____________组成的。通电后水发生____________变化,变化前后发生改变的是___________(填序号)。
①元素种类 ②原子个数 ③分子种类 ④各原子质量
【答案】气泡 使带火星的木条复燃 燃烧 氧气 氢气 氢元素和氧元素 化学 ③
【解析】
如图所示,电解水实验中,通电后电极上出现气泡,并汇集到试管上端。正极端的试管内产生的气体能使带火星的木条复燃,负极端的试管内产生的气体能燃烧;则正极端的试管内产生的气体是氧气,负极端的试管内产生的气体是氢气,说明水是由氢元素和氧元素组成的。通电后,生成了新的物质,水发生化学变化;化学变化过程就是旧的分子分成原子,原子再重新组合成新的分子的过程,所以,原子是化学变化中最小的微粒,故化学变化前后,发生改变的是分子的种类,而原子的种类、个数、质量都不改变,元素是同类原子的总称,元素的种类也不变。故选③。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案【题目】为了测定实验室中KClO3样品的纯度,某学习小组取2.5g该样品与0.5gMnO2混合,加热该混合物t1时间后(假设杂质不参加反应),冷却,称量剩余固体的质量,重复以上操作,依次称得加热t1、t2、t3、t4时间后剩余固体的质量,记录数据如下表所示。
加热时间 | t1 | t2 | t3 | t4 |
剩余固体质量/g | 2.48 | 2.34 | 2.04 | 2.04 |
请仔细分析实验数据,回答下列问题:
(1)在_____________时间后,该样品中的KClO3已经完全反应。
(2)完全反应后产生O2的质量是_______________。
(3)该样品中KClO3的质量是______。
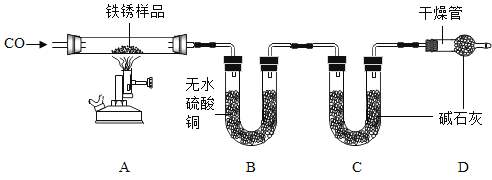
【题目】某兴趣小组根据下列装置进行实验,请你参与并回答:

(1)②仪器的名称是_____。
(2)若用A装置制取氧气,则①中可观察到的现象是_____(任答一点);写出该反应的化学方程式_____。
(3)B和C装置均可制取CO2,与B相比较,C的主要优点_____。
(4)常用金属锌和稀硫酸反应制取。若实验室要制取少量氢气最好选择发生装置_____(填字母);若用试管排空气法收集氢气,请在D处方框中画出装置图_____(只画试管和导气管)。
(5)某研究性学习小组为了测定某矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4份,进行实验,结果如下:(杂质不与稀盐酸反应)
实 验 | 1 | 2 | 3 | 4 |
加入样品的质量/g | 5 | 10 | 15 | 20 |
生成CO2的质量/g | 1.76 | 3.52 | 4.4 | m |
①表格中m的数值是_____。
②求石灰石中碳酸钙的质量分数_____。