题目内容
【题目】请结合下图回答问题。
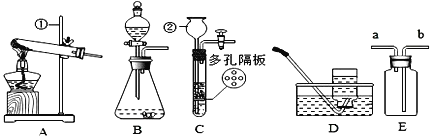
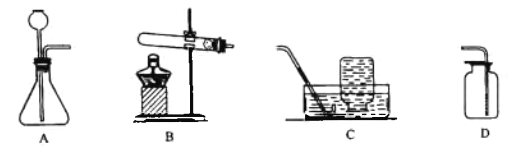
(1)仪器②的名称:____________。
(2)用氯酸钾和二氧化锰制取氧气,可选用装置____________(选填序号)和装置D组合,反应的化学方程式为____________,二氧化锰的作用是____________,若用B和D组合制取氧气,其反应的化学方程式为_____。
(3)实验室可用装置B或C制H2,C装置相对于B的优点有______,用E装置收集H2,气体应从______(选填“a”或“b”)端通入。
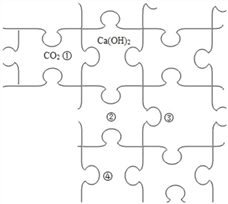
(4)某些大理石中含少量硫化物,使制得的CO2中混有H2S等气体。欲获取纯净、干燥的CO2,设计实验如下:
查阅资料:I.H2S能与NaOH、CuSO4等物质反应。
Ⅱ.CO2中混有的HC1气体可用饱和NaHCO3溶液吸收。
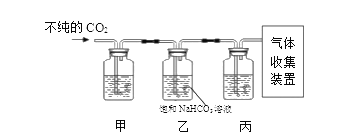
①装置甲中所盛试剂应选用____________(填字母)。
a.浓硫酸 b.NaOH溶液 c.澄清石灰水 d.CuSO4溶液
②装置丙的作用是____________。
【答案】 长颈漏斗 A 2KClO3![]() 2KCl+3O2↑ 催化 2H2O2
2KCl+3O2↑ 催化 2H2O2![]() 2H2O+O2↑ 能够控制反应的进行与停止 a d 干燥CO2或除去水蒸气
2H2O+O2↑ 能够控制反应的进行与停止 a d 干燥CO2或除去水蒸气
【解析】本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的除杂等,综合性比较强。气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关。
(1)仪器②的名称是长颈漏斗;
(2)用氯酸钾和二氧化锰制氧气需要加热,发生装置选用A,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,化学方程式是:2KClO3 ![]() 2KCl+3O2↑;其中二氧化锰起催化作用;若用B和D组合制取氧气,是用过氧化氢与二氧化锰混合生成氧气和水反应的化学方程式为2H2O2
2KCl+3O2↑;其中二氧化锰起催化作用;若用B和D组合制取氧气,是用过氧化氢与二氧化锰混合生成氧气和水反应的化学方程式为2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(3)C装置相对于B的优点有:控制反应的发生和停止;氢气的密度比空气小,用E装置收集H2,气体应从a端通入;
(4)①装置甲中所盛试剂是为除去H2S,浓硫酸不能除去H2S,不能选用,NaOH溶液和澄清石灰水都能与二氧化碳反应不能选用,CuSO4溶液能吸收H2S,不能与二氧化碳反应,能选用,故选D;
②从装置乙中出来的气体中含有水蒸气,欲获取纯净、干燥的CO2,装置丙的作用是干燥CO2或除去水蒸气。

 同步练习强化拓展系列答案
同步练习强化拓展系列答案【题目】徐州地区石灰石资源丰富。某化学兴趣小组称取4.0g石灰石样品,把40g稀盐酸分4次加入样品中(假设杂质不反应也不溶解),得实验数据如下:
稀盐酸的用量 | 剩余固体的质量 |
第一次加入10g | 3.0g |
第二次加入10g | 2.0g |
第三次加入10g | 1.0g |
第四次加入10g | 0.6g |
请计算:
(1)4.0g石灰石样品中碳酸钙的质量是____g。
(2)10g稀盐酸能与_____g碳酸钙正好完全反应。
(3)求稀盐酸的溶质质量分数为_________(写出计算过程,结果精确到0.1%)