题目内容
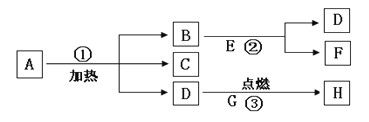
【题目】工业上以粗盐(含少量MgCl2、CaCl2杂质)为原料,利用电解饱和食盐水的方法制备NaOH,其简要工艺流程如下:
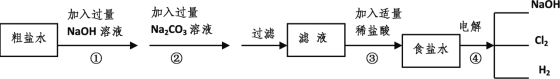
(1)步骤①反应方程式为MgCl2 + 2NaOH = Mg(OH)2↓ +2NaCl,其基本反应类型是_____
(2)写出步骤②中反应的化学方程式是________。
(3)步骤③中加入适量稀盐酸的目的是________。
(4)写出步骤④中反应的化学方程式________。
【答案】复分解反应 Na2CO3 + CaCl2== CaCO3↓+ 2NaCl 除掉过量的氢氧化钠和碳酸钠 2NaCl+2H2O![]() 2NaOH+ H2↑+ Cl2↑
2NaOH+ H2↑+ Cl2↑
【解析】
(1)步骤①反应方程式为MgCl2 + 2NaOH = Mg(OH)2↓ +2NaCl,其基本反应类型是由两种化合物相互交换成分生成两种新的化合物的复分解反应;
(2)步骤②中反应是碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,化学方程式是Na2CO3 + CaCl2== CaCO3↓+ 2NaCl;
(3)步骤③中加入适量稀盐酸的目的是除掉过量的氢氧化钠和碳酸钠,防止氯化钠不纯;
(4)步骤④中反应是氯化钠溶液在通电条件下反应生成氯气、氢气、氢氧化钠,化学方程式2NaCl+2H2O![]() 2NaOH+ H2↑+ Cl2↑。
2NaOH+ H2↑+ Cl2↑。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目