题目内容
【题目】分类、类比是学习化学常用的方法。
(1)化学实验常伴随着颜色的改变、放出气体、生成沉淀等明显的实验现象。下列实验根据实验现象的不同,把其中一个实验与其他三个实验区分出来,这个实验是__________,理由是__________。
A 镁与稀盐酸反应
镁与稀盐酸反应
B 铜与硝酸银溶液反应
铜与硝酸银溶液反应
C 铁与稀硫酸反应
铁与稀硫酸反应
D 铝与硫酸铜溶液反应
铝与硫酸铜溶液反应
(2)很多碱可以分解,但其分解难易程度和产物不同:金属的活动性越强,分解所需条件越高,Cu(OH)2、Fe(OH)3 加热就可以分解,生成与碱同价态的金属氧化物和水;而 NaOH 等强碱只有电解才能分解, 生成相应的金属单质、水和氧气。根据上述信息, 写出 KOH 分解的化学方程式__________。
【答案】A 没有溶液颜色的变化,其他三个有溶液颜色的变化 ![]()
【解析】
镁和稀盐酸反应生成氯化镁和氢气,铜和硝酸银反应生成硝酸铜和银,铁与稀硫酸反应生成硫酸亚铁和氢气,铝和硫酸铜反应生成硫酸铝和铜,氢氧化钾通电分解生成钾、水和氧气。
(1)A中镁和稀盐酸反应生成氯化镁和氢气,放出气体;B中铜和硝酸银反应生成硝酸铜和银,溶液变成蓝色;C中铁与稀硫酸反应生成硫酸亚铁和氢气,溶液变成浅绿色,放出气体;D中铝和硫酸铜反应生成硫酸铝和铜,溶液变为无色,故根据实验现象的不同,把其中一个实验与其他三个实验区分出来,这个实验是A,理由是A没有溶液颜色的变化,其他三个有溶液颜色的变化。
(2) NaOH 等强碱只有电解才能分解, 生成相应的金属单质、水和氧气,则 KOH 通电分解生成钾、水和氧气,反应的化学方程式为![]() 。
。

 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案【题目】“暖贴”是我们冬天常用的一种用品。某化学兴趣小组对暖贴中成分及发热原理展开了探究。
(1)暖贴中含有铁粉、活性炭、水、氯化钠等物质,从物质的分类看,其中含有的化合物有盐类和______。
(2)检验配料中含有铁粉。
用磁铁吸引黑色粉末,发现部分黑色粉末被吸引。取少量附着在磁铁上的粉末于试管中加入适量的______。通过观察到的现象是产生气泡、______,得出配料中含有铁粉。
(3)检验配料中含有活性炭。
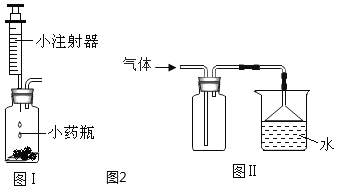
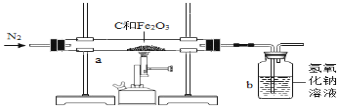
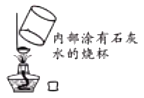
“暖贴”中的活性炭是利用它能______大量潮湿的空气,为铁粉氧化提供条件。小明用图中所示方法实验。将暖贴里的物质放在燃烧匙中,在酒精灯上加热。观察到烧杯内壁变浑浊,说明含有活性炭。此方案______![]() 填“可行”或“不可行”
填“可行”或“不可行”![]() 。若可行,写出其理论依据,若不可行,请你写出原因______。
。若可行,写出其理论依据,若不可行,请你写出原因______。
(4)探究暖贴中活性炭、食盐和水等物质的作用,实验数据如下。
实验编号 | 实验药品及用量 | 反应时间 | 温度上升值 | ||||
铁粉 | 活性炭 | 食盐 | 水 | ||||
对照组 | 1 | 0.2 | 0.1 | 5 | 10 | 58 | |
实验组 | 1 | 0 | 0.2 | 0.1 | 5 | 10 | 0 |
2 | 1 | 0 | 0.1 | 5 | 10 | 2.7 | |
3 | 1 | 0.2 | 0.1 | 0 | 10 | 4.5 | |
4 | 1 | 0.2 | 0 | 5 | 10 | 20 | |
①分析实验组4与对照组的数据,可说明______。
②其发热原理是:使用时,撕开其表面隔气膜,让空气与潮湿的铁发生反应生成氢氧化铁而放热,请写出化学方程式______。有同学认为袋中的物质铁可以用作食品包装的双吸剂,请你再写出一种常用的食品干燥剂是______。