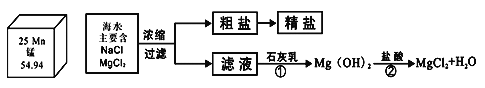
题目内容
【题目】下图为某化学反应的微观模拟示意图,下列有关该反应的说法中,不正确的是
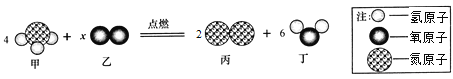
A. 反应前后氮元素的化合价发生改变 B. 该反应属于置换反应
C. 参加反应的甲、乙两物质的质量比为17:24 D. 图示中x的值为2
【答案】D
【解析】A. 单质中元素的化合价为零,化合物中元素的化合价代数和为零,故反应前后氮元素的化合价发生改变 ; B. 一种单质和一种化合物生成另一种单质和另一种化合物的反应叫置换反应,该反应属于置换反应;C. 据质量守恒定律可知反应前后原子的种类个数不变,所以甲、乙的分子个数比为4:3,参加反应的甲、乙两物质的质量比,17×4:32×3=17:24 D. 甲、乙的分子个数比为4:3,图示中x的值为3。选D

【题目】同学们运用对比的学习方法探究碱的性质。
实验一 | 实验二 |
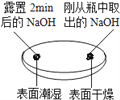
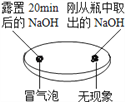
观察固体表面
| 向两块固体表面滴加稀盐酸
|
(1)由上图实验一、二可知,氢氧化钠会吸收空气的_________,因此要密封保存。
(2)同学们看到盛有NaOH的试剂瓶上标注着“NaOH含量不少于96.0%”,开始如下探究:
【提出问题】氢氧化钠中含有什么杂质?
【查阅资料】工业制取NaOH的反应原理是:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑,然后蒸发溶剂获得NaOH固体(在化工生产中,原料往往不能完全转化为产品)。
2NaOH+H2↑+Cl2↑,然后蒸发溶剂获得NaOH固体(在化工生产中,原料往往不能完全转化为产品)。
【提出猜想】杂质为_________和NaCl。理由是氢氧化钠暴露在空气中变质和氯化钠没有完全转化为氢氧化钠。
【实验探究】取样溶于水,并分成两份。
实验步骤 | 实验现象 | 实验结论 |
步骤①:向一份溶液中滴加酚酞试剂 | 溶液变红 | 猜想正确 |
步骤②:向另一份溶液中滴加过量___________ | 产生气泡 | |
步骤③:向步骤②所得溶液中滴加___________溶液 | 产生白色沉淀 |
【实验反思】
Ⅰ.上述实验中步骤 ___(填写序号)是没有必要进行的;
Ⅱ.步骤②所得溶液中的溶质除NaCl外,还有____________。
【题目】兴趣小组分析了用硫铁矿烧渣(主要成份Fe2O3、Fe3O4、FeO等)制备铁红(Fe2O3) 的流程图并进行了铁红性质实验。

(1)实验室完成操作1,用到的铁制仪器是_____________。
(2)你认为对气体C最佳的处理方法是___________。
A.冷却后排入空气 B.燃烧后排放 C.再通入反应炉
(3)在生成K2SO4的这个反应中,相关物质的溶解度如下表。
物质 | KCl | K2SO4 | NH4Cl | (NH4)2SO4 |
溶解度/g(20℃) | 34.2 | 11.1 | 37.2 | 75.4 |
你认为该反应在常温下能实现的原因是___________________。
(4)洗涤干燥得到K2SO4晶体时,可选用下列_______(填字母)洗涤剂;
A.KCl的饱和溶液 B.水 C.K2SO4的饱和溶液
为检验K2SO4晶体是否洗涤干净,可取最后一次洗涤液,先加入_______(选填序号,下同),振荡、静置,再向上层清液中滴加________,观察现象即可判断。(已知硫酸银在水中微溶,以沉淀形式存在)
A.AgNO3溶液 B.过量的BaCl2溶液 C.过量的Ba(NO3)2溶液
(5)在空气中煅烧FeCO3即FeCO3与空气中的氧气反应生成Fe2O3与CO2,试写出该反应的化学反应方程式为___________________