题目内容
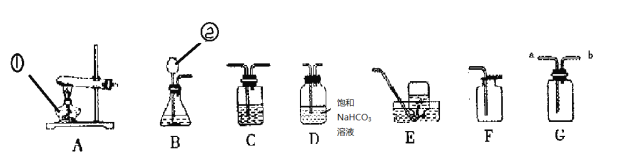
【题目】(8分)实验室制取气体常常用到下列装置,根据给出的装置回答下列问题:

(1)写出标号仪器的名称:② .
(2)若该实验选择装置A来制取氧气,请写出该反应的化学方程式 .
(3)若选择高锰酸钾制取并收集较纯净的氧气,则应选择装置组合 .该套装置有一处不足的地方,请你指出并加以改进: ;
(4)用图F装置收集氧气:若广口瓶充满水来收集氧气,气体应从 (填“a”或“b”)端通入;
(5)通过查阅资料得知:①氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,其水溶液称为氨水;②氨水能使无色酚酞试液变红;③实验室用氯化铵(NH4Cl)和熟石灰两种固体反应物混合加热可制取氨气,同时生成氯化钙和水。则实验 室制取氨气的装置组合可以选用 。小芳将收满氨气的集气瓶倒扣在滴有无色酚酞的水中,观察到的现象是______________、_______ _____。
【答案】(1)集气瓶
(2)2H2O2 MnO2 2H2O+ O2↑
(3)BC 试管口应塞一团棉花
(4)b
(5)BE 或BF 集气瓶内液面上升 无色酚酞变红
【解析】
试题分析:(1)常见仪器的识记:集气瓶
(2)气体发生装置的选择依据:反应物的状态和反应条件,装置A适用于固体和液体在常温下反应,故反应的化学方程式为:2H2O2 MnO2 2H2O+ O2↑
(3)选择高锰酸钾制取氧气是固体和固体在加热条件下反应,故选择发生装置B,要收集较纯净的氧气,应采用排水法收集,故收集装置选C;该套装置有一处不足的地方,改进措施:试管口应塞一团棉花
(4)用图F装置收集氧气:若广口瓶充满水来收集氧气,即排水法收集气体,气体应固定从短管通入,即b端
(5)实验室用氯化铵(NH4Cl)和熟石灰两种固体反应物混合加热可制取氨气,故发生装置选B,而收集装置的选择依据:气体的密度和溶解性,氨气(NH3)密度比空气小,极易溶于水,故只能采用向下排空气法,即装置E;将收满氨气的集气瓶倒扣在滴有无色酚酞的水中,观察到的现象是:集气瓶内液面上升;氨水能使无色酚酞试液变红,故无色酚酞变红

【题目】甲、乙、丙、丁表示四种物质,其微观示意图见下表,甲和乙在一定条件下反应生成丙和丁.
物质 | 甲 | 乙 | 丙 | 丁 |
|
微观示意图 |
|
|
|
|
下列说法正确的是
A.甲、丁的化学式相同
B.只有丙物质属于单质
C.若16g乙参加反应,则生成的丙质量为32g
D.反应中,反应物分子中所含氧原子总数是生成物分子中所含氧原子总数的2倍
【题目】(14分)请完成下列相关内容:
Ⅰ.实验表明,大多数金属都能与氧气发生反应,但反应的难易和剧烈程度是不同的。
(1)铁在潮湿的空气中易生锈,铁锈的主要成分为 ;铁在氧气中能剧烈燃烧,现象为 ,反应的化学方程式为 。
(2)铜在潮湿的空气中也容易锈蚀生成铜绿,其主要成分是碱式碳酸铜[Cu2(OH)2CO3],铜锈蚀除了与氧气有关外,还与空气中的 有关。
(3)铝在空气中具有很好的抗腐蚀性能,其原因是 。
Ⅱ.过氧化钠(Na2O2)是一种淡黄色固体,能与水或二氧化碳反应放出氧气。实验室有一瓶放置了较长时间的过氧化钠粉末,已知发生了部分变质,同学们取3.00g变质粉末决定探究其中的成分。

【提出问题】变质的过氧化钠粉末中有哪些成分?
【查阅资料】2Na2O2+2H2O═4NaOH+O2↑
2Na2O2+2CO2═2Na2CO3+O2
【猜想与假设】(1)粉末成分是Na2O2和NaOH的混合物
(2)粉末成分是 的混合物
(3)粉末成分是Na2O2、NaOH 和Na2CO3的混合物
……
【实验探究】
实验步骤 | 实验现象 | 实验结论 |
①取3.00g变质粉末于一支大试管中,加入适量的水,共收集到0.32g气体,然后用带火星木条检验生成的气体。 | 固体完全溶解, | 该固体样品中含有Na2O2,其质量为 g。 |
②继续向上述试管中加入足量的石灰水,充分反应。 | 化学方程式 。 | |
③将②中物质过滤,得到滤渣,将其洗涤、干燥并称量,得固体1.00g。 |
【得出结论】同学们经过实验和计算分析,该固体样品中所含物质有 。
【拓展应用】过氧化钠(Na2O2)是供氧设备中常用的供氧剂。若将15.6g过氧化钠与足量的二氧化碳充分反应,理论上生成的氧气质量是多少?(写出计算过程)。