题目内容
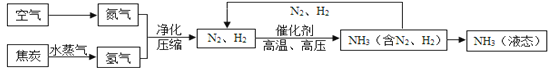
【题目】(10分)我国著名化学家侯德榜发明的“联合制碱法”主要原理是:I.向浓氨水中通入足量的CO2,使氨气、水和CO2发生化合反应而生成NH4HCO3溶液;II.向所得溶液中加入食盐细粒,充分搅拌,会析出溶解度较小的小苏打固体并得到化肥溶液;III.加热析出的固体制取纯碱。此法经过调整并应用于化工产业,某化工企业的工艺流程示意图如下:

请完成下列填空:
(1)“联合制碱原理II”中发生反应的化学方程式为 。
(2)在如图的流程中,先加Ca(OH)2溶液的目的是 ,再加入Na2CO3溶液的目的是 。
(3)“操作1”的名称是 ,“氨化溶液”后,溶液的pH 7(填:“大于”、“小于”或“等于”),从而有利于吸收“气体A”,气体A为 (填名称)。
(4)利用“270℃以上小苏打完全分解,纯碱受热不分解”的性质,化学兴趣小组的同学对实验室所购纯碱(假设所含杂质均为小苏打)进行了如下实验:称取20.00g干燥的固体样品放入坩埚,300℃恒温加热至质量不变,在干燥器中冷却后称量残留固体质量为19.38g。
根据题目所给信息,计算该样品中纯碱的质量分数(写出计算过程)。
【答案】(1)NH4HCO3+NaCl====NaHCO3↓+ NH4Cl
(2)将氯化镁转化为氢氧化镁沉淀;将氯化钙和多余的氢氧化钙除去
(3)过滤,大于,二氧化碳
(4)91.6%
【解析】
试题分析:(1)由描述2可知,碳酸氢铵与氯化钠反应生成碳酸氢钠和氯化铵:
NH4HCO3+NaCl====NaHCO3↓+ NH4Cl ;
(2)由流程图可知,粗盐中含有氯化钙和氯化镁,加入氢氧化钙后,氢氧化钙可与氯化镁反应生成氢氧化镁沉淀;再加入碳酸钠,碳酸钠能与氯化钙反应生成碳酸钙沉淀;
(3)通过操作1将固体和液体分离了,故是过滤操作;“氨化溶液”后,溶液中含有氨水,呈碱性,PH>7;气体A将溶液碳酸化,故是通入二氧化碳;
(4)碳酸氢钠分解生成碳酸钠、水和二氧化碳,由于生成的二氧化碳会逸散到空气中,而在干燥器中冷却后称量残留固体质量为19.38g,故生成的二氧化碳的质量=20.00g-19.38g=0.62g,利用化学方程式根据发碳酸钠与二氧化碳反应的质量比即可计算出碳酸氢钠的质量;
设碳酸氢钠的质量为x,
2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
168 44
X 0.62g
168/44 =x/0.62g x=1.68g
故样品中碳酸钠的质量=20g-1.68g=18.32g
样品中碳酸钠的质量分数=18.32g/20g ×100%=91.6%
答:略