题目内容
葡萄糖是生命体所需能量的主要来源.提出问题:葡萄糖燃烧的产物是CO2和H2O,由此能否推断葡萄糖是由碳元素和氢元素组成的有机物?
实验设计:为了确定葡萄糖的元素组成,某小组设计了如下实验(其中浓硫酸、无水CaCl2均为常用干燥剂,部分固定装置省略,假设每个装置中均吸收完全或反应完全).

| 小贴士 含碳元素的化合物完全燃烧生成CO2 、H2O,不完全燃烧时生成CO、CO2 和H2O |
(2)装置B处Fe2O3可能发生的化学反应的方程式为 .
方案评价:
用充有空气的储气球代替制备氧气的装置,是否更有利于实验的进行,为什么? .(填“是”或“否”及理由)
数据处理:下表是同学们填写的实验报告,请你帮助完成.
| 实验事实 | 数据分析及结论 |
| 1.8g葡萄糖完全燃烧,得到2.64g CO2和1.08g H2O | 结论:葡萄糖含有 元素 数据分析的依据是 . |
【答案】分析:(1)根据浓硫酸的吸水性回答
(2)葡萄糖发生氧化反应时可能生成一氧化碳,一氧化碳与氧化铁反应
方案评价:根据空气中也含有二氧化碳回答.
数据处理:根据质量守恒定律,由葡萄糖的质量和生成物的总质量求出参加反应的氧气的质量,再根据二氧化碳和水中的氧元素的质量求出总氧元素的质量,并把它与氧气的质量对比,看葡萄糖中是否含有氧元素.
讨论交流:根据氢氧化钠固体的吸水性及与二氧化碳反应分析
解答:解:(1)氧气中可能含有水蒸气,浓硫酸有吸水性,可以吸收氧气中的水蒸气,以便进行后续实验.
(2)葡萄糖燃烧时可能也产生一氧化碳,氧化铁可与一氧化碳反应,化学方程式为3CO+Fe2O3 2Fe+3CO2
2Fe+3CO2
方案评价:空气中也含有二氧化碳,会影响葡萄糖燃烧生成的二氧化碳质量的测定.
数据处理:根据质量守恒定律,葡萄糖燃烧需O2:2.64g+1.08g-1.8g=1.92g,而2.64gCO2中氧的质量为2.64g×32÷44=1.92g,1.08gH2O中氧的质量为1.08g×16÷18=0.96g,即生成物中总的氧元素质量为1.92g+0.96g=2.88g,2.88g>1.92g,所以,葡萄糖含有C、H、O三种元素.
讨论交流:从实验装置图可以看出C装置氯化钙是吸收生成的水,实验装置D中氢氧化钠是吸收生成的二氧化碳,E中NaOH固体是吸收空气中的二氧化碳和水,防止进入D装置对实验结果造成干扰.
故答案为:
(1)吸收从随着氧气溢出的水蒸气,防止影响C处的称量结果.
(2)3CO+Fe2O3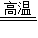 2Fe+3CO2
2Fe+3CO2
方案评价:否,空气中的CO2会干扰实验结果的测定
数据处理:葡萄糖含有C、H、O三种元素,依据是质量守恒定律或者“元素的种类和质量在化学变化前后不变”
讨论交流:
D中NaOH吸收葡萄糖燃烧产生的二氧化碳;E中的NaOH吸收空气中的二氧化碳和水,以减少误差
点评:本题是一道综合实验题,主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.
(2)葡萄糖发生氧化反应时可能生成一氧化碳,一氧化碳与氧化铁反应
方案评价:根据空气中也含有二氧化碳回答.
数据处理:根据质量守恒定律,由葡萄糖的质量和生成物的总质量求出参加反应的氧气的质量,再根据二氧化碳和水中的氧元素的质量求出总氧元素的质量,并把它与氧气的质量对比,看葡萄糖中是否含有氧元素.
讨论交流:根据氢氧化钠固体的吸水性及与二氧化碳反应分析
解答:解:(1)氧气中可能含有水蒸气,浓硫酸有吸水性,可以吸收氧气中的水蒸气,以便进行后续实验.
(2)葡萄糖燃烧时可能也产生一氧化碳,氧化铁可与一氧化碳反应,化学方程式为3CO+Fe2O3
 2Fe+3CO2
2Fe+3CO2方案评价:空气中也含有二氧化碳,会影响葡萄糖燃烧生成的二氧化碳质量的测定.
数据处理:根据质量守恒定律,葡萄糖燃烧需O2:2.64g+1.08g-1.8g=1.92g,而2.64gCO2中氧的质量为2.64g×32÷44=1.92g,1.08gH2O中氧的质量为1.08g×16÷18=0.96g,即生成物中总的氧元素质量为1.92g+0.96g=2.88g,2.88g>1.92g,所以,葡萄糖含有C、H、O三种元素.
讨论交流:从实验装置图可以看出C装置氯化钙是吸收生成的水,实验装置D中氢氧化钠是吸收生成的二氧化碳,E中NaOH固体是吸收空气中的二氧化碳和水,防止进入D装置对实验结果造成干扰.
故答案为:
(1)吸收从随着氧气溢出的水蒸气,防止影响C处的称量结果.
(2)3CO+Fe2O3
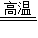 2Fe+3CO2
2Fe+3CO2方案评价:否,空气中的CO2会干扰实验结果的测定
数据处理:葡萄糖含有C、H、O三种元素,依据是质量守恒定律或者“元素的种类和质量在化学变化前后不变”
讨论交流:
D中NaOH吸收葡萄糖燃烧产生的二氧化碳;E中的NaOH吸收空气中的二氧化碳和水,以减少误差
点评:本题是一道综合实验题,主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
葡萄糖是生命体所需能量的主要来源.
[提出问题]葡萄糖在完全燃烧时产物是CO2和H2O,由此能否证明葡萄糖是只由碳元素和氢元素组成的有机物?
[实验设计]为了确定葡萄糖的元素组成,某小组设计了如下实验(无水CaCl2吸水,不吸收CO2).
(1)装置B中浓硫酸的作用是______.
(2)装置C处氧化铜的作用,是将葡萄糖可能不完全燃烧产生的少量CO气体______.
[数据处理]
(3)下表是同学们填写的实验报告,请你帮助完成.
[方案评价]
(4)装置D、E不能调换顺序,理由是______.
(5)装置F是保护装置,它能有效防止空气中的水分和CO2气体进入装置,影响测量结果.如果没有此保护装置,测量出的CO2质量会______(填“偏大”或“偏小”).
[提出问题]葡萄糖在完全燃烧时产物是CO2和H2O,由此能否证明葡萄糖是只由碳元素和氢元素组成的有机物?
[实验设计]为了确定葡萄糖的元素组成,某小组设计了如下实验(无水CaCl2吸水,不吸收CO2).

(1)装置B中浓硫酸的作用是______.
(2)装置C处氧化铜的作用,是将葡萄糖可能不完全燃烧产生的少量CO气体______.
[数据处理]
(3)下表是同学们填写的实验报告,请你帮助完成.
| 实验事实 | 数据分析及结论 |
| 1.8g葡萄糖完全燃烧后,D装置增重1.08g,E装置增重2.64g | 数据分析:1.8g葡萄糖含有C元素 ______g、H元素______g 结论:葡萄糖含有C、H、O三种元素 |
(4)装置D、E不能调换顺序,理由是______.
(5)装置F是保护装置,它能有效防止空气中的水分和CO2气体进入装置,影响测量结果.如果没有此保护装置,测量出的CO2质量会______(填“偏大”或“偏小”).


