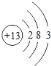题目内容
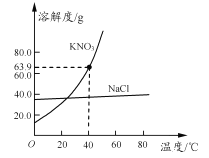
【题目】氯化钠和硝酸钾两种固体物质的溶解度曲线如图所示。下列说法正确的是
A. 硝酸钾的溶解度大于氯化钠的溶解度
B. 常用冷却结晶的方法从氯化钠溶液中获得其晶体
C. 40℃时,将30g硝酸钾晶体放入50g水中,充分搅拌后,所得溶液的溶质质量分数为37.5%
D. 将20℃的硝酸钾饱和溶液升温至60℃,溶液的溶质质量分数增大(忽略水分蒸发)
【答案】C
【解析】
A、比较不同物质间的溶解度,必须限定同一温度下,选项错误;B、根据图像,氯化钠溶解度随温度变化不明显,故采用蒸发结晶的方法获得晶体,选项错误;C、根据图像,40℃时,硝酸钾的溶解度为63.9g,故30g硝酸钾可完全溶于50g水中形成不饱和溶液,其质量分数为![]() ×100%=37.5%,选项正确;D、硝酸钾的溶解度随温度升高而明显变大,故将20℃的硝酸钾饱和溶液升温至60℃,溶液变为不饱和溶液,溶质和溶剂质量均没有变化,故质量分数不变,选项错误。故本题选C。
×100%=37.5%,选项正确;D、硝酸钾的溶解度随温度升高而明显变大,故将20℃的硝酸钾饱和溶液升温至60℃,溶液变为不饱和溶液,溶质和溶剂质量均没有变化,故质量分数不变,选项错误。故本题选C。

练习册系列答案
相关题目
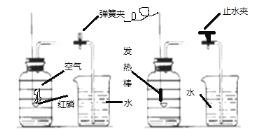
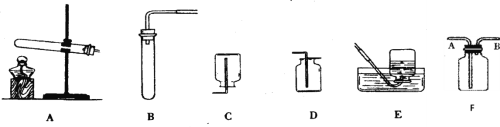
【题目】根据下列数据及实验装置图(所有夹持仪器均省略),回答下列问题:
物质 | 着火点 | 酒精灯的 火焰温度 |
白磷 | 500℃ | |
红磷 |
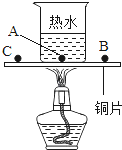
(1)在铜片上,A和C点为白磷;B点为红磷,用酒精灯对准A加热,最先发生燃烧的是(填字母,下同)________;一定不会发生燃烧的是________.
(2)将一支充满氧气的试管倒扣在(1)中“一定不会燃烧”的物质上面,现象是________;写出该反应的化学方程式 ________.
(3)烧杯中热水的作用是________.