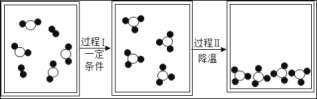
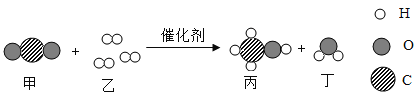
题目内容
【题目】碳酸钠和氯化钠、氢氧化钙三种物质(不含结晶水)的溶解度曲线如下图所示,下列叙述正确的是( )
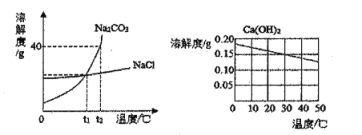
A. t1℃时,Na2CO3和NaCl的溶质质量相等
B. t2℃时,Na2CO3的饱和溶液中溶质质量分数为40%
C. 向40℃时的饱和澄清石灰水降温到20℃,溶质质量分数不变
D. 要从Na2CO3饱和溶液中得到碳酸钠晶体,最后用蒸发结晶的方法
【答案】C
【解析】
A、t1℃时,Na2CO3和NaCl的溶解度相同,但溶液的质量不确定,无法比较溶质质量的大小,故A错误;
B、t2℃时,Na2CO3的溶解度是40g,饱和溶液中溶质质量分数为:![]() ×100%≈28.6%;故B错误;
×100%≈28.6%;故B错误;
C、由于氢氧化钙的溶解度随温度的降低而增大,所以将40℃时的饱和澄清石灰水降温到20℃,溶质质量分数不变,故C正确;
D、由于Na2CO3溶随温度的变化而变化较大,要从饱和Na2CO3溶液中得到碳酸钠晶体,最好用降温结晶的方法,故D错误。
故选:C。

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案【题目】空气中氧气含量测定的再认识:
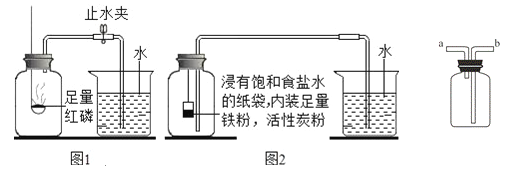
【实验回顾】如图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置。
(1)写出红磷燃烧的文字表达式: 。
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内 减小,烧杯中水倒吸到集气瓶.若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量。
【问题提出】有实验资料表明:燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧,因此通过上述实验,测量结果与理论值误差较大。
【实验改进】
Ⅰ、根据铁在空气中生锈的原理设计如图2实验装置,再次测定空气中氧气含量。装置中的饱和食盐水、活性炭会加速铁生锈。
Ⅱ、测得实验数据如下表:
测量项目 | 实验前 | 实验后 | |
烧杯中水的 体积 | 烧杯中剩余的 体积 | 集气瓶(扣除内容物)和导管的 容积 | |
体积/mL | 80.0 | 54.5 | 126.0 |
【交流表达】(1)铁生锈过程中发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁,写出该反应的文字表达式: 。
(2)根据表中数据计算,改进实验后测得的空气中氧气的体积分数是 (计算结果精确到0.1%)。
(3)从实验原理角度分析,改进后的实验结果比前者准确度更高的原因是:
① ;② 。