��Ŀ����
����Ŀ����ϸ̼��ƿ�����������Ƭ������Ȳ�Ʒ������̼����������ϸ̼��Ƶ���Ҫ����ʾ����ͼ��
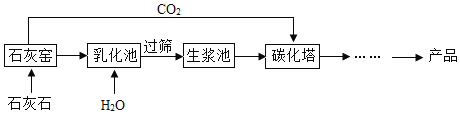
��1���黯���У���ʯ����ˮ������Ӧ���仯ѧ����ʽΪ_______________________��
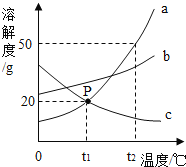
��2����ɸ��Ŀ��������_______������ڡ���С�ڡ���ɸ��ֱ���Ŀ�����
��3��ʯ��Ҥ�����ղ�������ͨ��̼�����Ƴɳ�ϸ̼��ƣ��ⲽ�������ŵ���______��
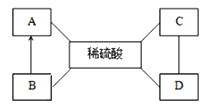
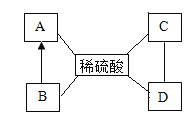
����ͼ�dz��л�ѧ�г�����һЩ���ʼ���ת����ϵ������A��E��GΪ���ʣ�MΪ����ɫ���塣
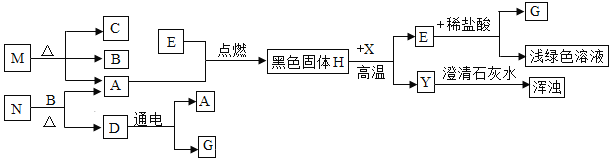
�ش��������⣺
��1��H�Ļ�ѧʽ_________��
��2��E��ϡ���ᷴӦ�Ļ�����Ӧ������____________��Ӧ��
��3��д������ת���Ļ�ѧ����ʽ��
��M��A+B+C��___________________________________��
��Y+ʯ��ˮ��_____________________________________��
���𰸡�CaO+H2O=Ca(OH)2 ���� ��ʡԭ�ϡ�����CO2�Ի�����Ӱ�죨�������ɣ� Fe3O4 �û� ![]() CO2+Ca(OH)2=CaCO3��+H2O
CO2+Ca(OH)2=CaCO3��+H2O
��������
��
��1����ʯ����ˮ��Ӧ�����������ƣ���Ӧ�Ļ�ѧ����ʽΪ��CaO+H2O=Ca(OH)2��
��2��������ɸ���黯�ر�Ϊ�������أ���ɸ��Ŀ�������ش���ɸ��ֱ���Ŀ�����
��3��ʯ��Ҥ�����ղ�������ͨ��̼�����Ƴɳ�ϸ̼��ƣ���ʡԭ�ϡ�����CO2�Ի�����Ӱ�죨�������ɣ���
��
A��E��GΪ���ʣ�Y��ʹ����ʯ��ˮ����ǣ�����Y�Ƕ�����̼��E��ϡ���ᷴӦ����dz��ɫ��Һ������ϡ���ᷴӦ�����Ȼ��������������Ȼ�������Һ��dz��ɫ������E������G��������A������ȼ�����ɺ�ɫ����H������������ȼ����������������������A��������H��������������������������X��Ӧ�����ɶ�����̼��������������һ����̼�ڸ������������Ͷ�����̼������X��һ����̼��Dͨ�������������������ˮͨ��ֽ���������������������D��ˮ��N��B��Ӧ������ˮ�����������������ڶ������̴������·ֽ�����ˮ������������N�ǹ���������Һ��B�Ƕ������̣�MΪ����ɫ���壬MΪ������أ�������ؼ��ȷֽ���������ء��������̺�������C������أ�������֤���Ƶ���ȷ��
�������Ϸ�����֪��
��1��H����������������ѧʽΪ��Fe3O4��
��2��E��ϡ���ᷴӦ������ϡ���ᷴӦ�����Ȼ��������������÷�Ӧ����һ�ֵ�����һ�ֻ����ﷴӦ��������һ�ֵ��ʺ���һ�ֻ�����ķ�Ӧ��������Ӧ�������û���Ӧ��
��3��д������ת���Ļ�ѧ����ʽ��
��M��A+B+C�Ǹ�������ڼ��ȵ���������������ء��������̺���������ѧ����ʽΪ��![]() ��
��
��Y+ʯ��ˮ��Ӧ�Ƕ�����̼���������Ʒ�Ӧ����̼��ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪ��CO2+Ca(OH)2=CaCO3��+H2O��

 һ��һ����ʱ���ϵ�д�
һ��һ����ʱ���ϵ�д�����Ŀ��Fenton�������ڴ������ѽ����л���Ĺ�ҵ��ˮ����ԭ��������Fe2+��H2O2��Ӧ�����ܽ�����Ⱦ��Ļ��Գɷ֡������ø÷��������л���Ⱦ��p-CP��̽���й����ضԽ��ⷴӦ���ʵ�Ӱ�졣ʵ��ʱ��p-CP�ij�ʼŨ����ͬ���¶Ⱥ�Ϊ25���40�森ʵ����p-CP��Ũ����ʱ��仯�Ĺ�ϵ��ͼ��
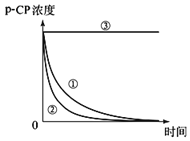
��ش�
��1�����������ʵ����Ʊ���
ʵ�� ��� | ʵ��Ŀ�� | �¶�/�� | pH | Ũ��/��mgL-1�� | |
H2O2 | Fe2+ | ||||
�� | Ϊ�ڢ��ṩ���� | 25 | 3 | 204 | 16.8 |
�� | ̽���¶ȶԽ��ⷴӦ���ʵ�Ӱ�� | ______ | 3 | 204 | 16.8 |
�� | ̽����ҺpH�Խ��ⷴӦ���ʵ�Ӱ�� | 25 | 10 | 204 | 16.8 |
��2��ʵ��١��ڱ����¶����ߣ����ⷴӦ����______��
��3����һ��ʵ�鷢�֣��¶ȹ���ʱ�����ⷴӦ���ѷ�������������Լ�H2O2�ĽǶȷ���ԭ��______��
��4��Ϊ�ⶨ��ͬʱ�����л��オ���Ũ�ȣ����ڲ�ͬʱ��ӷ�Ӧ����ȡ������ʹ��ȡ��Ʒ�еĽ��ⷴӦ����ֹͣ������ͼʾ��Ϣ����д��Ѹ��ֹͣ��Ӧ��һ�ַ�����______��
����Ŀ����1��ʵ���ǿ�ѧ̽������Ҫ�ֶΣ��밴Ҫ����д�����
ʵ������ | �����ᾧ | ϡ��Ũ���� |
ʵ����� |
|
|
�������� | �ٵ��������г���_____ʱ��ֹͣ���ȡ� | ���ձ�������A��������_____�� |
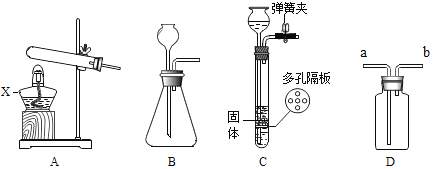
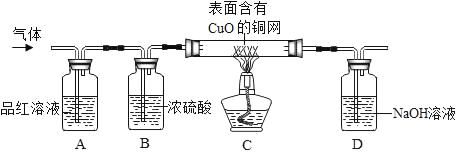
��2����ͼ��ʵ������ȡ���ռ������װ�ã��밴Ҫ��ش��������⡣
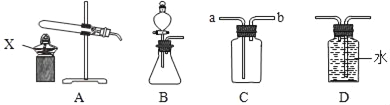
������X��������_____��
��ʵ�����ø��������ȡ���ռ��ϴ�����������Ӧѡ�õķ���װ�ú��ռ�װ�õ������_____������ĸ�����÷�Ӧ�Ļ�ѧ����ʽ��_____��
��ʵ�����ռ�CO2ʱ��ѡ��Cװ�ö���ѡ��Dװ�õ�������_____��CO2����Ӧ��Cװ�õ�_____�����a����b�������롣