题目内容
【题目】如图是三种物质的溶解度曲线,分析曲线得到的信息中,错误的是
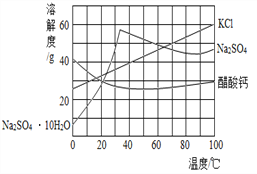
A. 约在64℃时,KCl和Na2SO4的溶解度相等
B. 在40℃时,40gKCl固体溶于60g水得到40%的KCl溶液
C. 在室温至100℃区间,随温度升高,Na2SO4的溶解度先增大后减小,醋酸钙则相反
D. 分离含少量KCl的溶液,采用先蒸发浓缩,后降温结晶的方法
【答案】B
【解析】A、由溶解度曲线可知,约在64℃时,KCl和Na2SO4有相交点,即溶解度相等,正确;B、在40℃时,氯化钾的溶解度为40g,即该温度时,100g水中溶解度40g氯化钾固体前后形成饱和溶液,那么60g水中最多溶解24g,溶质的质量分数=![]() =28.6%,错误;C、由溶解度曲线可知,在室温至100℃区间,随温度升高,Na2SO4的溶解度先增大后减小,醋酸钙则相反,正确;D、氯化钾的溶解度随温度的变化变化较大,分离含少量KCl的溶液,采用先蒸发浓缩使其变成饱和溶液,再采用降温结晶的方法即可分离出氯化钾,正确。故选B。
=28.6%,错误;C、由溶解度曲线可知,在室温至100℃区间,随温度升高,Na2SO4的溶解度先增大后减小,醋酸钙则相反,正确;D、氯化钾的溶解度随温度的变化变化较大,分离含少量KCl的溶液,采用先蒸发浓缩使其变成饱和溶液,再采用降温结晶的方法即可分离出氯化钾,正确。故选B。

练习册系列答案
相关题目