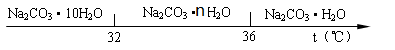题目内容
用括号内物质不能一次性区别开下列各组物质的是
| A.CaO、CaCO3、KCl 三种固体(水) |
| B.CaCl2、Na2CO3、K2SO4三种溶液 (Ba(OH)2溶液) |
| C.Cu、Fe、CuO三种固体(稀盐酸) |
| D.CuCl2、NaNO3、K2CO3三种溶液 (Ca(OH)2溶液) |
B
试题分析:A.加入水,放热的是氧化钙,固体溶解的是氯化钾,固体不溶的是碳酸钙,现象不同,可以鉴别; B.加入氢氧化钡溶液,碳酸钠和氢氧化钡反应产生白色沉淀,硫酸钾和氢氧化钡反应产生白色沉淀,现象相同,无法鉴别碳酸钠和硫酸钾; C. 铜不与稀盐酸发生反应,铁与盐酸能反应生成氯化亚铁并产生氢气,氧化铜与盐酸反应生成蓝色的氯化铜溶液,现象不同,故可以使用稀盐酸鉴别;D.氯化铜溶液本身是蓝色的,观察颜色能直接鉴别出来,剩余的两种溶液加入氢氧化钙溶液,能产生白色沉淀的是碳酸钾,无现象的是硝酸钠,现象不同,可以鉴别.

练习册系列答案
相关题目
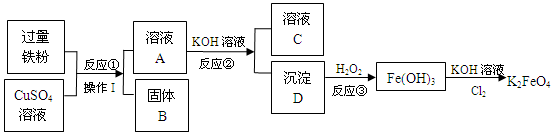
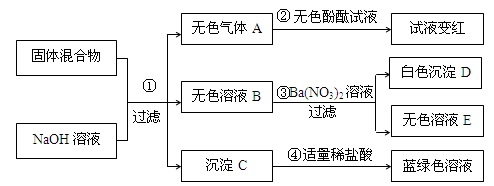

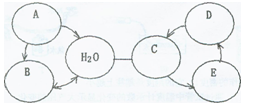

 ②2NaHCO3 Na2CO3+H2O+CO2↑
②2NaHCO3 Na2CO3+H2O+CO2↑