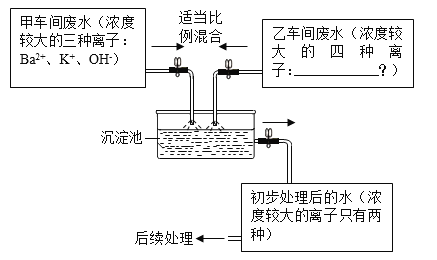
题目内容
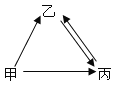
【题目】甲、乙、丙均含有同种元素,有下图所示的转化关系 (“→”表示反应一步实现,部分物质和反应条件已略去)。按要求回答问题。
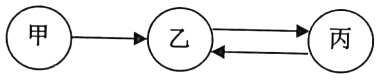
(1)若甲、乙为组成元素相同的化合物,丙为单质,则“甲→乙”的化学反应方程式为___________。
(2)若甲为单质,乙、丙为组成元素相同的化合物,且乙的相对分子质量小于丙。写出一个“乙→丙”的非化合反应的化学方程式______________________。
【答案】2CO+O2![]() 2CO2或2H2O2
2CO2或2H2O2![]() 2H2O+O2
2H2O+O2![]() (任意一个即可) CO+CuO
(任意一个即可) CO+CuO![]() Cu+CO2
Cu+CO2
【解析】
(1)因为甲、乙为组成元素相同的化合物,丙为单质,甲乙丙含有同种元素,
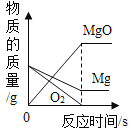
①甲乙丙可能为C、CO、CO2中的一种,丙为单质,所以丙是C,因为C+O2![]() CO2;CO2+2Mg
CO2;CO2+2Mg![]() 2MgO+C,丙和乙可以相互转化,所以乙是CO2,甲是CO,验证无误,推断正确。所以“甲→乙”的化学反应方程式为:2CO+O2
2MgO+C,丙和乙可以相互转化,所以乙是CO2,甲是CO,验证无误,推断正确。所以“甲→乙”的化学反应方程式为:2CO+O2![]() 2CO2;
2CO2;
②甲乙丙可能为H、H2O、H2O2中的一种,丙为单质,所以丙是H2,H2+O2![]() H2O;2H2O
H2O;2H2O![]() 2H2
2H2![]() +O2
+O2![]() , 丙和乙可以相互转化,所以乙是H2O,甲是H2O2,验证无误,推断正确。所以“甲→乙”的化学反应方程式为:2H2O2
, 丙和乙可以相互转化,所以乙是H2O,甲是H2O2,验证无误,推断正确。所以“甲→乙”的化学反应方程式为:2H2O2![]() 2H2O+O2
2H2O+O2![]() 。
。
故答案为:2CO+O2![]() 2CO2或2H2O2
2CO2或2H2O2![]() 2H2O+O2
2H2O+O2![]() (任意一个即可)
(任意一个即可)
(2)甲为单质,乙、丙为组成元素相同的化合物,且乙的相对分子质量小于丙。则甲可能为C,乙可能为CO,丙可能为CO2,验证无误,推断正确。“乙→丙”的非化合反应为CO还原CuO,化学方程式为CO+CuO![]() Cu+CO2。
Cu+CO2。

 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
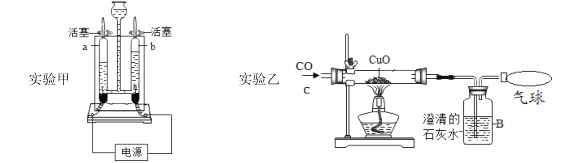
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案【题目】某研究小组用如图所示装置,探究能否用镁条代替红磷测定空气中氧气含量。

(提出猜想)
猜想1:可以代替,因为镁条与氧气反应后不会产生气体
猜想2:不能代替,因为镁条可能会与空气中的其他成分发生反应
(进行实验)
步骤 | 实验操作 | 实验现象 |
Ⅰ | 组装好装置后,打开止水夹,手捂集气瓶,一段时间后,松开手 | 烧杯中导管口有气泡冒出,松手后,烧杯中导管末端有一段液柱 |
Ⅱ | 关闭止水夹,点燃镁条,迅速伸入集气瓶中,塞好塞子 | 镁条燃烧,放出大量热,发出耀眼白光,生成大量白烟,剩余固体为白色带状物还夹杂着极少量淡黄色的固体 |
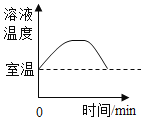
Ⅲ | 冷却至室温,打开止水夹 | 烧杯中水从导管进入集气瓶中,体积约为集气瓶体积的 |
(解释与结论)
(1)步骤Ⅰ的实验目的是_____。
(2)步骤Ⅱ中,关闭止水夹的目的是_____。
(3)根据实验现象中的_____(写一个即可)可以推测猜想2成立。
①(继续探究)经查阅资料得知氮化镁(Mg3N2)为淡黄色的固体,于是小晴猜想镁条还可能会与空气中的_____发生反应;
②(设计实验)她设计实验方案证明自己的猜想_____;
③(实验结论)镁条与氮气反应的化学方程式为:_____;
④(反思与评价)通过上述探究活动,你对燃烧有什么新的认识?_____。