题目内容
【题目】往AgNO3和Cu(NO3)2的混合液中加入一定量的铁粉,充分反应后过滤,向滤液中加入稀盐酸,产生白色沉淀。根据上述现象,你不能得出的结论是
A. 滤渣中一定有Fe粉B. 滤渣中一定有Ag粉
C. 滤液中一定有Fe2+D. 滤液中一定有Ag+、Cu2+
【答案】A
【解析】
往AgNO3和Cu(NO3)2的混合液中加入一定量的铁粉,铁先与硝酸银反应,再与硝酸铜反应。充分反应后过滤,向滤液中加入稀盐酸,产生白色沉淀,白色沉淀为氯化银,说明溶液中的硝酸银没有被完全反应完全,故得到滤液的溶质为硝酸银、硝酸铜和硝酸亚铁,滤渣为银,
故A错误,试题选A.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
【题目】某化学兴趣小组的同学按照课本上的实验装置做“测定空气中氧气的体积分数”实验(如图1所示),但测出的氧气的体积分数明显小于 ![]() .请你参与探究:
.请你参与探究: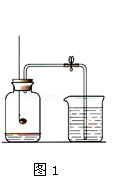
【提出问题】造成误差的原因是什么?如何改进课本上的实验装置?
【查阅资料】红磷、白磷的一些性质如下表:
颜色、状态 | 熔点/℃ | 着火点/℃ | 密度/(g/cm3) | |
红磷 | 暗红色固体 | 590 | 240 | 2.34 |
白磷 | 白色或黄色固体 | 44.1 | 40 | 1.82 |
(着火点也叫燃点,是可燃物燃烧需要的最低温度.)
(1)【猜想与假设】甲同学:可能是导管内原来含有空气,后来留有吸入的水,影响实验的准确性.
乙同学:可能是瓶内残留气体中还有氧气.
你还能作出的猜想是: .
(2)【交流与讨论】
1)丙同学认为用木炭代替红磷,就可以消除误差,大家认为他的猜想不合理,理由是 .
2)他们对课本上的实验装置进行了如图2所示的改进,为了确保实验的成功,在装药品之前应该 . 
①该实验的现象是 .
②甲同学提出应把红磷换为白磷,理由是 .
③通过粗铜丝来点燃玻璃管内的白磷,这利用了金属铜的性.与课本上的实验装置相比较,该装置的一个优点是 .