题目内容
【题目】实验室中有一包由KCl、MgSO4和CaCl2组成的固体混合物,某校研究性学习小组的同学为了得到纯净的 KCl,设计了如下实验方案:
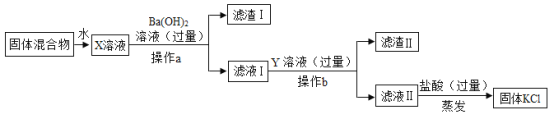
(1)操作a的名称是_____,其中玻璃棒的作用是_____。
(2)加入的Y溶液是_____;写出KCl的一种用途_____。
(3)加入氢氧化钡溶液发生的主要化学反应方程式为_____。
【答案】过滤 引流 K2CO3溶液 作钾肥 ![]()
【解析】
KCl、MgSO4和CaCl2组成的固体混合物溶解形成溶液X,向X溶液中加入过量Ba(OH)2溶液,生成BaSO4和Mg(OH)2沉淀,过滤之后,滤液I中含有KCl、CaCl2、Ba(OH)2,加入过量K2CO3溶液,生成CaCO3和BaCO3沉淀,过滤之后,滤液II中含有KCl、KOH、K2CO3,加入过量盐酸,最后溶液中只含有KCl和盐酸,经过蒸发结晶最终得到KCl固体。
(1)向X溶液中加入过量Ba(OH)2溶液,生成BaSO4和Mg(OH)2沉淀,所以操作a为过滤,将沉淀过滤,得到滤液;玻璃棒在过滤中的作用为引流;
(2)滤液I中含有KCl、CaCl2、Ba(OH)2,加入过量K2CO3溶液,可生成CaCO3和BaCO3沉淀,从而除去钙离子和钡离子;KCl可用作钾肥;
(3)向X溶液中加入过量Ba(OH)2溶液,生成BaSO4和Mg(OH)2沉淀,化学方程式为:![]() 。
。

 阅读快车系列答案
阅读快车系列答案【题目】实验室制备并收集二氧化碳
(1)选用药品。按下表进行实验,取等质量的大理石加入足量酸中(杂质不与酸反应), 产生二氧化碳的体积随时间变化曲线如下图所示:

实验编号 | 药品 |
Ⅰ | 块状大理石、10%H2SO4溶液 |
Ⅱ | 块状大理石、7%HCl溶液 |
Ⅲ | 大理石粉末、7%HCl溶液 |
(1)图中丙对应实验_____(填“Ⅰ”、“Ⅱ”或“III”)。确定用乙对应的药品制备并收集二氧化碳,相应的化学方程式是_____;不用甲对应的药品,理由是:_____。
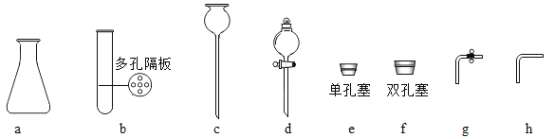
(2)搭建装置。组装可以控制反应速率的装置,应选用_____(填字母)。
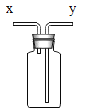
(3)收集气体。用下图装置收集时,空气从_____(填“x”或“y”)端排出。
(4)如果用(2)题搭建的装置制取氧气,发生的化学方程式是_____,其中固体物质在此反应中的作用是_____。