题目内容
【题目】已知金属R与硫酸铜溶液反应的化学方程式是:R+CuSO4=Cu+RSO4.则下列说法正确的是( )
A.该反应属于复分解反应 B.金属R的活泼性比Cu要强
C.该金属可以是金属铝 D.该金属一定是铁
【答案】B
【解析】根据金属R与硫酸铜反应的化学方程式:R+CuSO4═Cu+RSO4,该反应为金属单质R与化合物硫酸铜反应生成金属单质铜和化合物RSO4,属于置换反应;由于R能置换铜所以R排在铜前,而R还可以是排在铜前的其他金属可能是铁但不一定是铁;金属R在置换反应中表现为+2价,而金属铝只有+3价,金属R一定不是金属铝.综上所述,B正确;故选B.

【题目】某化学学习小组用如图装置来探究“影响H2O2分解速率”的因素。
(1)写出实验室用二氧化锰催化双氧水分解的化学方程式________________。
【提出问题】影响双氧水分解速率的因素有哪些?
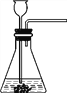
【猜想与假设】a.与双氧水浓度有关;b.与反应时温度有关。
【设计实验】
甲组同学有如下实验设计方案,见表(测量各生成一瓶相同体积O2所需要的时间)。
实验编号 | 温度 | 催化剂 | 浓度 | 时间 |
甲组实验Ⅰ | 25 ℃ | 1 g二氧化锰 | 10 mL 2%H2O2 | 115 s |
甲组实验Ⅱ | 25 ℃ | 1 g二氧化锰 | 10 mL 5%H2O2 | 35 s |
甲组实验Ⅲ | 35 ℃ | 1 g二氧化锰 | 10 mL 5%H2O2 | 15 s |
此实验中宜采用的气体收集方法是:________。
【收集证据】(2)要比较温度对双氧水分解快慢的影响,应选择的实验编号是________。
【得出结论】(3)根据上述实验得出的结论是________________________________________。
【继续探究】H2O2分解生成O2的快慢还与哪些因素有关?请你帮助他们继续探究。写出假设和实验方案。假设:________________________________________________;实验方案:___________________________________________。

(4)乙组同学研究酸、碱对H2O2分解速率的影响的变化曲线如图,请你观察右图回答问题。
①写出一条规律性结论:________________________________________________________;
②乙组提出可以用BaO2固体与硫酸溶液反应制H2O2(已知还生成另一种物质),其化学反应方程式为________________________________;支持这一方案的理由是________________________________。
