题目内容
【题目】实验室常用下列装置来制取氧气:
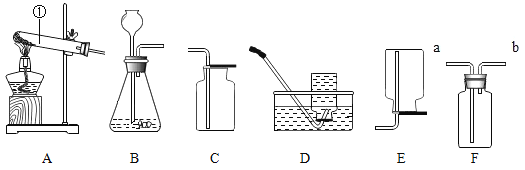
(1)写出仪器①的名称______________;
(2)用过氧化氢和二氧化锰来制取氧气时,可选用的发生装置是______(填序号),实验室用高锰酸钾制取氧气,可选用的发生装置是________。在加入药品之前应先______________, 该反应的文字或符号表达式:______________________反应后试管中残留固体是 __________ 物(填“混合物”或“纯净物”)
若选用D装置收集氧气时,下列实验操作不正确的是_____(填序号)。
a 加热前,将集气瓶装满水,用玻璃片盖住瓶口,倒立在盛水的水槽中
b 加热后,观察到水中导管口开始有气泡时,立即收集气体
c 待集气瓶里的水排完后,在水面下用玻璃片盖住瓶口,移出水槽正放在桌面上
d 实验结束后,先停止加热,后从水槽中取出导气管
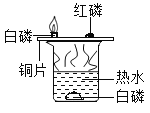
实验过程中小明同学观察到装置中的水变为红色,这是因为___________的缘故。
(3)用C装置收集氧气的依据是______________,这种收集方法检验氧气是否集满的方法是__________________________________________。
(4)F图是化学中的多功能瓶,可以有如下用途:
①可以用做排空气法收集氧气,氧气应从__________端进。
②医院里给病人输氧为了给氧气加湿和观察氧气的输出速度也可以在氧气瓶和病人吸氧管之间连接该装置,在集气瓶装半瓶水,将___________端接氧气钢瓶。
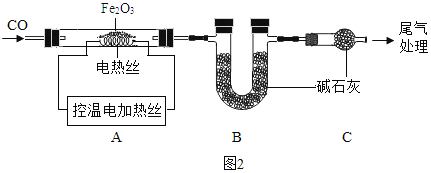
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3)。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小。NH3极易溶于水,其水溶液呈碱性。制取并收集NH3,应该从上图中选择的发生装置是_____________,收集装置是________。
【答案】试管 B A 检查装置的气密性 高锰酸钾![]() 锰酸钾+二氧化锰+氧气(或KMnO4
锰酸钾+二氧化锰+氧气(或KMnO4![]() K2MnO4 + MnO2 + O2) 混合物 bd 试管口没放棉花团,高锰酸钾颗粒通过导气管进入水中的缘故 氧气的密度比空气的密度大 将带火星的木条放在集气瓶口,观察木条是否复燃 a a A E
K2MnO4 + MnO2 + O2) 混合物 bd 试管口没放棉花团,高锰酸钾颗粒通过导气管进入水中的缘故 氧气的密度比空气的密度大 将带火星的木条放在集气瓶口,观察木条是否复燃 a a A E
【解析】
(1)仪器①是试管。
(2)固液常温反应制取气体,选择发生装置B,故用过氧化氢和二氧化锰来制取氧气时,可选用的发生装置是B;加热固体制取气体,选择发生装置A,故实验室用高锰酸钾制取氧气,可选用的发生装置是A。在加入药品之前应先检查装置的气密性,该反应的文字或符号表达式为:高锰酸钾![]() 锰酸钾+二氧化锰+氧气(或KMnO4
锰酸钾+二氧化锰+氧气(或KMnO4![]() K2MnO4 + MnO2 + O2),反应后试管中残留固体有生成的二氧化锰、锰酸钾,属于混合物。
K2MnO4 + MnO2 + O2),反应后试管中残留固体有生成的二氧化锰、锰酸钾,属于混合物。
a 加热前,将集气瓶装满水,用玻璃片盖住瓶口,倒立在盛水的水槽中,此选项正确;
b 加热后,观察到气泡连续均匀冒出时,立即收集气体,此选项错误;
c 待集气瓶里的水排完后,在水面下用玻璃片盖住瓶口,移出水槽正放在桌面上,此选项正确;
d 实验结束后,先从水槽中取出导气管,后停止加热,此选项错误。故选bd。
实验过程中小明同学观察到装置中的水变为红色,这是因为试管口没放棉花团,高锰酸钾颗粒通过导气管进入水中的缘故。
(3)用C装置收集氧气是向上排空气法收集氧气,依据是氧气的密度比空气的密度大,这种收集方法检验氧气是否集满的方法是将带火星的木条放在集气瓶口,如果带火星的木条复燃,则证明收集满了氧气。
(4)①由于氧气的密度比空气的密度大,F装置可以用做排空气法收集氧气,氧气应从a端进入。
②医院里给病人输氧为了给氧气加湿和观察氧气的输出速度也可以在氧气瓶和病人吸氧管之间连接该装置,在集气瓶中装半瓶水,将a端接氧气钢瓶,b端连接病人的吸氧管,否则水会被病人吸入体内。
(5)加热固体制取气体,选择发生装置A,故制取NH3选择发生装置A,NH3极易溶于水,不能用排水法收集,其密度比空气小,可用向下排空气法收集,故选E。

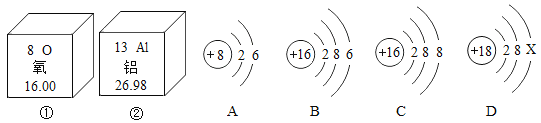
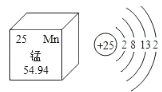
【题目】元素周期表是学习和研究化学的重要工具,可以从表中获得许多知识。图A(见下表)是元素周期表的一部分;图B和图C 是元素周期表中两种元素的原子结构示意图。请你根据图表回答下列问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
第二 周期 | 3 Li 锂 7 | 4 Be 铍 9 | …… | 5 B 硼 11 | ① | 7 N 氮 14 | 8 O 氧 16 | 9 F 氟 19 | 10 Ne 氖 20 |
第三 周期 | 11 Na 钠 23 | ② | …… | 13 Al 铝 27 | 14 Si 硅 28 | ③ | 16 S 硫 32 | 17 Cl 氯 35.5 | 18 Ar 氩 40 |

(1)从图A中找出原子序数为16的元素名称为_______;
(2)图C是某元素的原子结构示意图,该原子在化学反应中易______电子;
(3)图B是某元素的原子结构示意图,该元素在图A中的位置是______(选填①、②或③)。