题目内容
【题目】A~F是碳单质、氧化铜、二氧化碳、稀硫酸、氢氧化钡和氯化钡六种物质中的某一种,A、B都是黑色固体,E属于盐, 它们之间的相互关系如图所示(实连线“—”表示物质间能反应, 虚连线“”表示物质间不能反应)。请回答下列问题:

(1)C的化学式是________。
(2)A与B反应的化学方程式为__________。
(3)反应⑤:E与F反应的化学方程式为__,该反应与上图关系中___(从①~⑥中选填序号,⑤无需再选)反应都属于复分解反应。
(4)在上图中,三个虚线连接中存在转化关系的有(填物质化学式):________→_________。
【答案】CO2 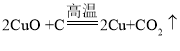
![]() ④⑥ CuO CO2
④⑥ CuO CO2
【解析】
A~F是碳单质、氧化铜、二氧化碳、稀硫酸、氢氧化钡和氯化钡六种物质中的某一种,A、B都是黑色固体,则A、B是碳或氧化铜,E属于盐,则E是氯化钡,E、F能反应,则F是稀硫酸,B、F能反应,则B是氧化铜,A是碳,A、C能反应,则C是二氧化碳,则D是氢氧化钡,代入验证正确;
(1)C是二氧化碳,化学式是CO2;
(2)A与B反应是高温条件下碳和氧化铜反应产生铜和二氧化碳,反应的化学方程式为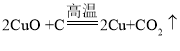 ;
;
(3)E与F反应是氯化钡与稀硫酸反应生成硫酸钡沉淀和盐酸,反应的化学方程式为![]() ,属于复分解反应;反应④为硫酸和氧化铜反应产生硫酸铜和水,反应⑥氢氧化钡与稀硫酸反应生成硫酸钡沉淀和水,也属于复分解反应,故填:④⑥;
,属于复分解反应;反应④为硫酸和氧化铜反应产生硫酸铜和水,反应⑥氢氧化钡与稀硫酸反应生成硫酸钡沉淀和水,也属于复分解反应,故填:④⑥;
(4)氧化铜和碳(或一氧化碳)高温(或加热)条件下反应,能生成二氧化碳,故存在转化关系的是:CuO→CO2;

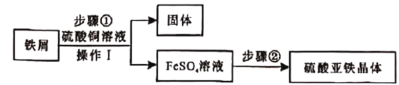
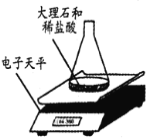
【题目】某同学对“影响稀盐酸和大理石反应快慢的因素”进行探究。选取的药品:成分相同的粉末状大理石、块状大理石两种样品;浓度为16%、9%的稀盐酸。采用控制变量法设计实验方案,以5分钟内收集到CO2的质量作为判断依据。已知稀盐酸足量且样品中杂质不与稀盐酸反应,实验装置如图。读取电子天平的示数,据此计算生成的CO2的质量,记录的数据如下表
实验序号 | 大理石 (各6g) | 稀盐酸的浓度 | 反应开始到5分钟产生CO2的质量 | 反应结束产生的CO2的质量 |
① | 块状 | 16% | 2.16 g | 2.2 g |
② | 块状 | 9% | 1.42 g | 2.2 g |
③ | 粉末 | 16% | 2.33 g | 2.2 g |
④ | 粉末 | 9% | 1.93 g | m 2g |
(1)稀盐酸的浓度对该反应快慢的影响: __________。
(2)实验过程中,通过观察如图装置中的哪一现象可判断反应结束__________。
(3)结合表格分析,实验④反应结束后m2的值________。
(4)探究大理石的颗粒大小对该反应快慢的影响,其实验序号分别是__________。