题目内容
【题目】某工厂排放的废液中含有Zn(NO3)2和AgNO3,为回收金属Ag,设计了下列方案:
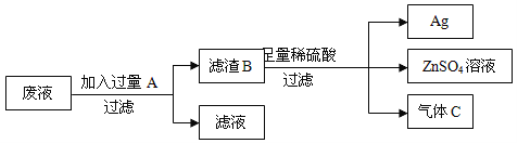
B中含有______________,气体C是________。
【答案】Zn、Ag H2
【解析】
金属活动顺序表:K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au,在金属活动顺序表中,排在氢前边的金属能和酸发生置换反应生成盐和氢气。金属的位置越靠前,金属的活动性越强。位置靠前的金属能将位于其后的金属从它的盐溶液中置换出来。某工厂排放的废液中含有Zn(NO3)2和AgNO3,现要回收金属Ag,根据流程图可知废液中加入过量的A,所以滤渣中剩余金属A和反应生成的金属,滤渣B中加入稀硫酸后,溶液为硫酸锌溶液,且生成气体,固体为银,所以可知滤渣为银和锌,锌和硫酸反应生成硫酸锌和氢气,银不与硫酸反应。故填:Zn、Ag;H2。

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
【题目】Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件。某化学兴趣小组的同学为了测定某黄铜的组成,取10g该黄铜样品于烧杯中,向其中分5次加入相同溶质质量分数的稀硫酸,使之充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于下表:
加入稀硫酸的质量(g) | 充分反应后剩余固体的质量(g) | |
第1次 | 10 | m |
第2次 | 10 | 7.4 |
第3次 | 10 | 6.1 |
第4次 | 10 | 5.6 |
第5次 | 10 | n |
试回答下列问题:
(1)从以上数据可知,最后剩余的5.6g固体的成分是_____;表格中,m=_____,n=_____。
(2)黄铜样品中锌的质量分数为_____。
(3)计算所用稀硫酸中硫酸的质量分数为_____。