题目内容
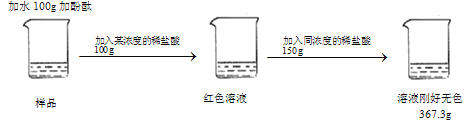
【题目】如图1所示是氢氧化钠溶液与盐酸反应的实验研究。
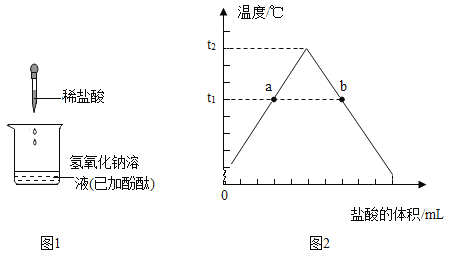
(1)图1中,证明氢氧化钠与盐酸发生中和反应的实验现象是______________。
(2)随着盐酸不断滴入,烧杯中溶液的pH逐渐_____________ (填“增大”“减小”或“不变”),该反应的化学方程式是______________。
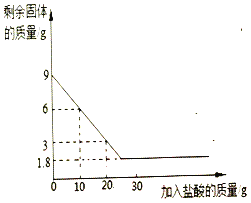
(3)随着盐酸不断滴入,烧杯中溶液温度变化如坐标图2所示。某时刻测得溶液的温度是t1℃,请判断b点对应的溶液中溶质是______________。
(4)当溶液的温度为t2℃时,证明溶液不含氢氧化钠的实验方法是______________。
【答案】溶液由红色变为无色 减小 NaOH+HCl═NaCl+H2O NaCl、HCl 向溶液中加一滴氢氧化钠溶液,溶液又变为红色(合理即可)
【解析】
(1)氢氧化钠溶液显碱性,能使无色的酚酞试液变红色,滴加稀盐酸后,二者反应中和反应生成氯化钠和水,恰好完全反应时溶液呈中性,溶液由红色变成无色;故填:溶液由红色变成无色;
(2)随着盐酸不断滴入,盐酸与氢氧化钠发生中和反应生成氯化钠和水,所以烧杯中溶液的pH逐渐减小,故填:减小; NaOH+HCl═NaCl+H2O;
(3)由图象可知,b点时,滴加到盐酸已经过量,此时溶液显酸性,溶液中的溶质是氯化钠和氯化氢;故填:NaCl、HCl;
(4)氢氧化钠溶液显碱性,能使无色的酚酞试液变红色,所以可向向溶液中加一滴氢氧化钠溶液,溶液又变为红色,证明溶液不含氢氧化钠;故填:向溶液中加一滴氢氧化钠溶液,溶液又变为红色。

 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案【题目】小刚在化学实验室发现,盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末。小刚叫来小军和小红,共同探究这种白色粉末的成分。
(提出问题)白色粉末的成分是什么?
(进行猜想)他们依据所学的化学知识,对这种白色粉末的成分作了如下猜想:①可能是NaOH;②可能是Na2CO3;③可能是NaOH与Na2CO3的混合物。
(设计实验)
(1)为了验证猜想,小军做了下面的实验:
序号 | 实验操作 | 实验现象 | 结论 |
1 | 取少量白色粉末,滴加足量稀盐酸 | 气体生成 | 猜想______不正确 |
2 | 取少量白色粉末溶于水,向所得溶液中滴加无色酚酞溶液 | ________________ | 猜想③正确 |
(反思改进)
(2)小红认为小军实验2不能得出猜想③正确,请说明理由__________________
(3)小刚认为小红说的对,为了验证猜想③,设计以下实验:
序号 | 实验操作 | 实验现象 | 结论 |
Ⅰ | 取少量白色粉末溶于水,向所得溶液中滴加过量 _________溶液 | 产生白色沉淀 | 猜想③正确 |
Ⅱ | 取实验Ⅰ的上清液,向溶液中滴加FeCl3溶液 | _______________ |
请你写出实验Ⅰ中反应的化学方程式____________。
(反思应用)氢氧化钠易潮解,且容易与空气中CO2发生反应,所以氢氧化钠固体应该_________保存。