题目内容
某化学研究性学习小组欲测定实验室里一瓶久置的NaOH固体是否变质。
【作出猜想】猜想I:没变质,全部是NaOH;猜想II:_▲_;猜想Ⅲ:完全变质,全部是Na2CO3。
【查阅资料】①已知反应: BaCl2+Na2CO3=2NaCl+BaCO3↓
BaCl2+Na2CO3=2NaCl+BaCO3↓
②部分盐溶液在常温下的pH如下:
| 盐溶液 | NaCI | Na2CO3 | BaCl2 |
| pH | 等于7 | 大于 | 等于7 |
【设计方案并进行实验】请你与他们一起共同完成,并回答所给问题。
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述氢氧化钠固体样品10.0g溶于50ml水配成溶液,向溶液中滴加氯化钡溶液至过量,充分反应后,静置。 | ▲ | 说明久置固体中,一定含有Na2CO3 |
| ②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块pH试纸上,与标准比色卡对比,测出pH | pH=11 | 说明久置固体中,还一定含有 ▲ |
上述步骤① 中,滴加过量BaCl2溶液的目的是 ▲ 。
中,滴加过量BaCl2溶液的目的是 ▲ 。
【实验结论】通过实验,说明上述猜想中 ▲ 是正确的。
是正确的。
【拓展】该小组同学为测定出该NaOH固体的变质程度,继续将上述白色沉淀过滤、洗净、干燥,称得其质量为3.94g,求原试剂中NaOH的质 量分数。(写出计算过程,假定试剂中无其它杂质)。
量分数。(写出计算过程,假定试剂中无其它杂质)。
作出猜想】部分变质,是NaOH和Na2CO3;
【设计方案并进行实验】产生白色沉淀。NaOH
证明并除去Na2CO3。
【实验结论】II。 【拓展】78.8%(3分)

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
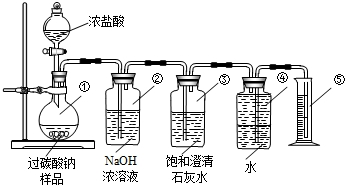
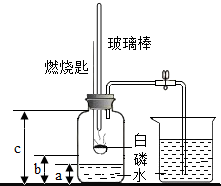 某化学研究性学习小组在学习了“空气中氧气含量测定”实验的基础上,改进了教材中的实验,设计出如图所示的实验装置.
某化学研究性学习小组在学习了“空气中氧气含量测定”实验的基础上,改进了教材中的实验,设计出如图所示的实验装置.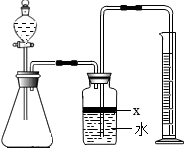 氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,某化学研究性学习小组设计并完成了如下实验.
氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,某化学研究性学习小组设计并完成了如下实验.