题目内容
 按如图组装仪器,关闭止水夹,通电使红磷燃烧.回答下列问题:
按如图组装仪器,关闭止水夹,通电使红磷燃烧.回答下列问题:(1)红磷燃烧的化学方程式:
(2)冷却后,松开止水夹,你观察到的现象为
(3)该装置改进后的优点是
分析:(1)红磷燃烧生成了五氧化二磷,根据反应写出反应的方程式;红磷过量,能将瓶内的氧气全部消耗掉.
(2)根据瓶内压强的变化分析.
(3)根据改进后装置的特点分析优点.
(2)根据瓶内压强的变化分析.
(3)根据改进后装置的特点分析优点.
解答:解:(1)红磷燃烧生成了五氧化二磷,反应写出反应的方程式是:4P+5O2
2P2O5,该实验中红磷需稍过量,目的是:将集气瓶内的氧气全部消耗掉;
(2)由于红磷燃烧生成了五氧化二磷固体,消耗了瓶内的氧气,瓶内的压强减小.所以,冷却后,松开止水夹,你观察到的现象为:烧杯里的水倒吸到集气瓶内(或烧杯的水面下降),集气瓶中的水约占集气瓶容积的
,由此可以得出:空气中氧气的体积分数的
.
(3)通电的方法引燃红磷,不需要打开瓶塞,空气出不来也进不去,测量比较准确;用酒精灯引燃红磷,红磷燃烧生成的五氧化二磷会污染空气;由于磷燃烧放出大量的热,打开瓶塞时容易使空气受热而逸出,测定结果不准确.所以优点为:误差少,无污染.
故答为:(1)4P+5O2
2P2O5,将集气瓶内的氧气全部消耗掉;(2)烧杯里的水倒吸到集气瓶内,集气瓶中的水约占集气瓶容积的
,
;(3)误差少,无污染.
| ||
(2)由于红磷燃烧生成了五氧化二磷固体,消耗了瓶内的氧气,瓶内的压强减小.所以,冷却后,松开止水夹,你观察到的现象为:烧杯里的水倒吸到集气瓶内(或烧杯的水面下降),集气瓶中的水约占集气瓶容积的
| 1 |
| 5 |
| 1 |
| 5 |
(3)通电的方法引燃红磷,不需要打开瓶塞,空气出不来也进不去,测量比较准确;用酒精灯引燃红磷,红磷燃烧生成的五氧化二磷会污染空气;由于磷燃烧放出大量的热,打开瓶塞时容易使空气受热而逸出,测定结果不准确.所以优点为:误差少,无污染.
故答为:(1)4P+5O2
| ||
| 1 |
| 5 |
| 1 |
| 5 |
点评:空气是人类宝贵的自然资源,在中考中占有重要的地位,特别是空气中氧气含量的测定,要注意测定原理、实验关键、现象和结论等内容的考查.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
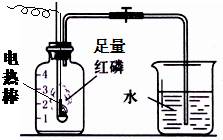 按如图组装仪器,关闭止水夹,通电使红磷燃烧.请回答下列问题:
按如图组装仪器,关闭止水夹,通电使红磷燃烧.请回答下列问题: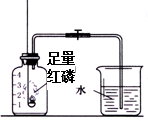 按如图组装仪器,关闭止水夹,点燃红磷并迅速伸入集气瓶中.请回答下列问题:
按如图组装仪器,关闭止水夹,点燃红磷并迅速伸入集气瓶中.请回答下列问题: