题目内容
【题目】室温下,小雪同学将10%的氢氧化钠溶液,逐滴加入到100g硫酸铜溶液中。
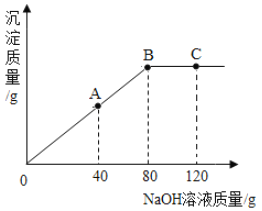
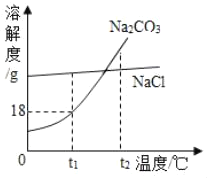
①当滴入氢氧化钠溶液40g时(即图中A点),烧杯中溶液里含的溶质为(写化学式)_____。
②该反应过程中,观察到的一个明显反应现象是_____。
③当滴入10%氢氧化钠溶液80g时(即图中B点),恰好完全反应,试通过计算,求此时所得不饱和溶液的质量_____(计算结果精确到0.1g)。
【答案】CuSO4、Na2SO4 生成蓝色沉淀 170.2g
【解析】
①当滴入氢氧化钠溶液40g时(即图中A点),此时硫酸铜尚未完全反应,所以烧杯中溶液里含的溶质为剩余的硫酸铜和生成的硫酸钠,对应的化学式为 CuSO4、Na2SO4。
②该反应过程中,观察到的一个明显反应现象是 生成蓝色沉淀。
③当滴入10%氢氧化钠溶液80g时(即图中B点),恰好完全反应,此时消耗的氢氧化钠的质量为10%×80g=8g
设生成的氢氧化铜的质量为y
CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
80 98
8g y
![]() =
=![]()
y=9.8g
此时所得不饱和溶液的质量100g+80g﹣9.8g=170.2g。

 名校课堂系列答案
名校课堂系列答案【题目】某兴趣小组在空气中点燃镁条时发现:生成的白色固体物质中夹杂着少量的淡黄色固体。为了探究其原因,小组成员进行了以下探究活动:
(提出问题)淡黄色固体物质的成分是什么?
(查阅资料通过查阅资料,记录了下列几种物质的颜色:
物质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
颜色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
小组成员一致认为产物中一定不含有氯化镁,理由是______。
(提出猜想)淡黄色的固体可能是______。
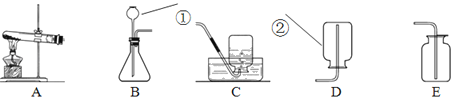
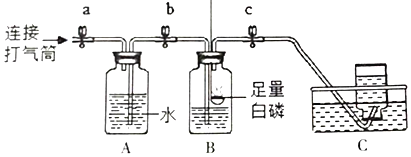
(实验探究](1)按如图所示装置收集氮气
①关闭a、b、c,用凸透镜聚光引燃白磷,待白磷不再燃烧并冷却至室温。
②打开a、b,使用打气筒进行充气,A中的水进入B时,打开c,继续充气。C中收集到N2.选用排水法收集氮气的原因是______。
(2)实验验证的方法是将燃烧的镁条伸入集气瓶,若观察到______现象,则证明淡黄色固体是Mg3N2。
(实验结论)猜想是正确的,镁条在空气中燃烧的有关化学反应方程式是______。
(实验反思)本探究活动对物质燃烧新的认识是______。