题目内容
【题目】现有符号①2O ②N2 ③2O3 ④2CO ⑤2N3- ⑥SO42- ⑦3Fe3+ ⑧H2O ⑨![]() ,其中数字“2”表示的含义不同,下列判断正确的是( )
,其中数字“2”表示的含义不同,下列判断正确的是( )
A. 表示分子个数:①③ B. 表示离子个数:⑤⑦
C. 表示原子个数:②④⑧ D. 表示化合价:⑥⑨
【答案】B
【解析】A、标在分子符号前面的数字表示分子的个数,③2O3、④2CO中的“2”分别表示2个臭氧分子、2个一氧化碳的分子,故错误;
B、标在离子符号前面的数字表示离子的个数,⑤2N3﹣⑦3Fe2+中的“2”分别表示氮离子的个数为2、“3”分别表示铁离子的个数为3,故正确;
C、标在元素符号前面的数字表示原子的个数,①2O中的“2”表示氧原子的个数为2;②N2、⑧H2O中的2分别表示1个氮分子中含有2个氮原子、1个水分子中含有2个氢原子;故错误;
D、标在元素符号正上方的数字表示元素的化合价,⑨![]() 中的2表示氧化镁中镁元素的化合价为+2价;故错误;
中的2表示氧化镁中镁元素的化合价为+2价;故错误;
故选:B.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
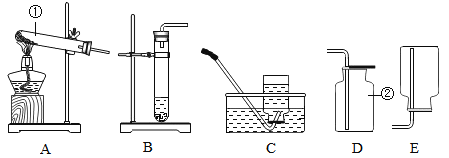
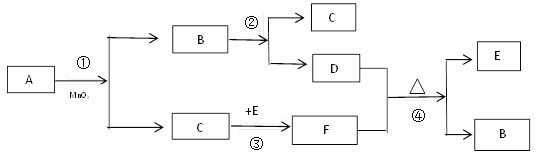
小学生10分钟应用题系列答案【题目】二百多年前,法国化学家拉瓦锡用定量的方法研究了空气的成分。仿照这个历史上著名实验的原理,我们可以用图1所示装置来测定空气中氧气的含量。

【提出问题】用红磷燃烧的方法为什么测出的氧气含量远低于21%?
【分析讨论】(1)实验装置漏气;(2)________________,导致装置内氧气有剩余;(3)……
【实验与交流】在老师的指导下,同学们查阅了白磷、红磷等物质燃烧需要的最低含氧量如下:
资料1:
可燃物名称 | 红磷 | 白磷 | 蜡烛 |
最低含氧量/% | 8.0 | 4.0 | 16.0 |
甲、乙、丙三个小组分别用上述过量红磷、白磷、蜡烛三种物质进行该实验,用测氧气浓度的传感器测得反应后的氧气浓度分别为8.85%、3.21%、16.7%,数据与表中的理论值基本一致。其中蜡烛燃烧后用测一氧化碳浓度传感器测算一氧化碳浓度约为2%。
资料2:蜡烛或者木炭在密闭的集气瓶中燃烧,氧气浓度会不断变小,会有一氧化碳气体生成。常温下一氧化碳难溶于水,且不与澄清石灰水反应。根据以上信息回答下列问题:
(1)白磷和红磷相比,使用白磷能使结果更准确,其原因是_______________________。
(2)请写出红磷燃烧的化学方程式______________,该反应属于___________反应(填一种基本反应类型);有同学提议选用木炭替代红磷做实验,在集气瓶底部预先放少量澄清石灰水吸收生成的二氧化碳气体,小华觉得不可行,其主要原因是________________。
(3)兴趣小组用白磷代替红磷进行实验,已知化学反应前后元素种类和质量都不发生改变,若该实验中消耗的氧气质量为0.8克,则理论上生成的五氧化二磷的质量为______。
【实验拓展】某校研究性学习小组用下图装置进行镁条在空气中燃烧的实验。燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%。
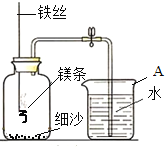
(4)实验过程中,若弹簧夹未夹紧,则进入集气瓶中的水会_______(选填“偏大”、“偏小”或“不变”)。
(5)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的_______,现进入集气瓶中水的体积约为其容积的 70%,根据空气的组成可推出减少的气体中还一定有氮气,其理由是______________________。
【提出问题】氮气是怎样减少的呢?
【作出假设】氮气是与镁条反应而减少的。
【查阅资料】
①镁条在空气中燃烧时,不仅与空气中的氧气反应生成氧化镁,还能与氮气反应生成氮化镁(氮化镁中氮元素的化合价为-3价),请写出镁条与氮气反应的化学方程式__________;
②镁条除了能与氮气反应,还可以在二氧化碳气体中燃烧生成碳和氧化镁,请你写出该反应的化学方程式___________
【验证实验】用坩埚钳夹持镁条,点燃后迅速伸入盛有氮气的集气瓶中,镁条燃烧,发出暗红色火焰,生成淡黄色粉末,并放出大量的热。
【得出结论】镁条能在氮气中燃烧生成固体氮化镁。
【实验反思】通过以上实验探究,我们可以知道用于测定空气中氧气含量所选用的药品,应符合的条件是____________________。
【题目】若将一定量的某中电池燃料R和氧气置于封闭的容器中,在一定条件下充分反应,测定反应前后各物质的质量如下表,不正确的是( )
物质 | R | 氧气 | 水 | 二氧化碳 |
反应前质量 | 8.0 | 9.6 | 0 | 0 |
反应后质量 | 待测 | 0 | 7.2 | 8.8 |
A. 表中待测的值为1.6 B. 物质中含有碳氢氧三种元素
C. 物质中碳氢质量比为3:1 D. 二氧化碳和水的分子个数比为1:3