题目内容
【题目】甲、乙、丙、丁4种物质在反应前后的质量关系如图所示,下列有关说法正确的是(____)
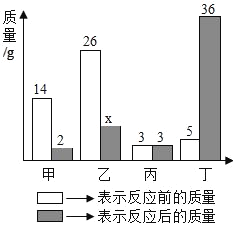
A 参加反应的甲和乙质量比为2:7
B 丙一定是该反应的催化剂
C 丁一定是化合物
D 该反应的基本反应类型是_____反应
【答案】C 化合
【解析】
甲、乙反应后质量减少,故甲、乙属于反应物,丁反应后质量增加,丁属于生成物,丙反应前后质量不变,丙可能是催化剂或不参与反应的杂质。
A、根据质量守恒定律,化学反应前后,物质的总质量不变,故14+26+5+3=2+x+3+36,x=7,故参加反应的甲和乙质量比为:(14-2):(26-7)=12:19,不符合题意;
B、丙反应前后质量不变,丙可能是催化剂也可能是不参与反应的杂质,不符合题意;
C、甲、乙为反应物,丁为生成物,该反应属于化合反应,故丁一定是化合物,符合题意;
D、该反应符合“多变一”的特点,属于化合反应。
故选C,填化合。

【题目】根据物质的溶解度表和物质的溶解度曲线,回答问题。
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | 氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
硝酸钾 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
氢氧化钙 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 | |
(1)向20℃的氢氧化钙饱和溶液中加入少量生石灰,再冷却至20℃,此时溶液中溶质的质量比加入生石灰前溶液中溶质的质量_____(填“增大”“不变”或“减小”)。
(2)混有少量氯化钠的硝酸钾固体,加水配成80℃的硝酸钾饱和溶液,再冷却至20℃,析出晶体并得到溶液。下列有关说法中正确的是_____(填字母)。
A 析出的晶体中不一定含有硝酸钾
B 所得溶液一定是硝酸钾饱和溶液
C 上述方法可以将两种物质完全分离
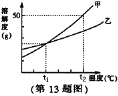
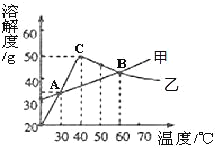
(3)将甲、乙饱和溶液从60℃降温到40℃,溶质的质量分数是:甲_____乙(填“>”、“=”、“<”)。
(4)等质量的甲、乙饱和溶液从30℃升温到60℃,为使其溶液恰好饱和,加入的甲、乙固体质量_____(填“相等”或“不相等”)。
【题目】某化学兴趣小组的同学,为了比较金属R与铁、铜的金属活动性强弱,进行如下探究活动:
[查阅资料]铁的活动性比铜强。
[进行猜想]对三种金属的活动性顺序做出如下猜想:
猜想一: R>Fe>Cu;
猜想二:_____
猜想三: Fe>Cu>R
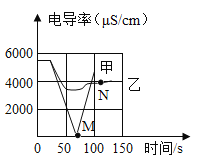
[收集证据]为了验证哪一种猜想成立,甲、乙、丙三位同学分别展开实验探究。
主要操作 | 主要现象 | 实验结论 | |
甲 | 将打磨好的R丝插入盛有硫酸铜溶液的试管中 | _____ | 猜想一正确 |
乙 | 将粗细相同打磨好的R丝、铁丝,分别插入体积和溶质质量分数都相同的稀盐酸中 | R 丝表面产生气泡速率比铁丝表面产生气泡速率_____(填“快”或“慢”) | |
丙 | 将粗细相同打磨好的R丝、铁丝,分别在空气中点燃 | R 丝在空气中剧烈燃烧,铁丝在空气中不燃烧 |
写出铁丝与稀盐酸反应的化学方程式_____。
[交流反思]三位同学交流讨论后认为,比较金属活动性强弱的方法有多种。
[归纳总结]他们总结得出比较金属活动性强弱的常见方法有:
(1)金属与氧气反应的难易和剧烈程度;
(2)金属与酸溶液是否反应或反应的剧烈程度;
(3)金属与_____是否反应。
【题目】自然界并不缺少镁,缺少的是发现镁的眼睛。某化学兴趣小组开启寻镁之旅,现邀请你参与并完成相关内容。
(1)第一站:初识金属镁。(①金属镁的物理性质:____(写一条);②金属镁的化学性质:镁能与氧气反应,反应的化学方程式为___.
(2)第二站:再遇金属镁。将打磨过的镁条放入稀盐酸中,反应现象是______。化学方程式为______。
(3)第三站:制备金属镁。小组同学模拟工业上从海水晒盐剩下的苦卤中提取镁,流程如下:
![]()
流程中X为________________.
(4)第四站:再探金属镁。
(提出问题)镁能否与热水反应?如果反应,产物是什么?
(相关信息)①Mg+2H2O=Mg(OH)2+H2↑②氢氧化镁在热水中能部分溶解。
实验操作 | 实验现象 | 实验结论 |
______ | _____ | 镁能与热水反应,生成氢氧化镁和氢气 |
(5)上述寻镁之旅中你收获到镁的化学性质有_______.