题目内容
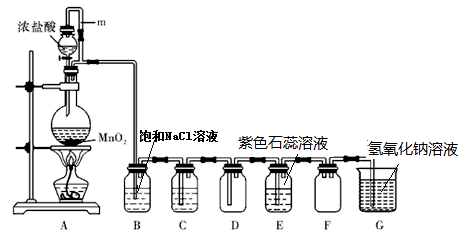
【题目】实验室常用下列装置来制取、收集气体.仪器b是分液漏斗,可通过旋转活塞分次滴加液体.请回答以下问题.
(1)仪器a、c的名称是:a , c .
(2)实验室用KMnO4制取O2 , 应选用的发生装置和收集装置的组合为(填字母序号),该发生装置的不足之处是 , 该反应的化学方程式是 . 收集装置的选择是由气体的性质决定的.既能用排水法也能用排空气法收集的气体一定具有的性质有(填数字序号)
①易溶于水 ②难溶于水 ③不与水反应 ④密度与空气接近 ⑤可与空气中某成分反应 ⑥有毒,是一种大气污染物
(3)某同学取一定浓度盐酸与石灰石反应,将生成的气体通入澄清石灰水中,始终未见浑浊,请将可能的原因填入下表,并用简单的实验进行验证:
可能的原因 | 实验步骤 | 实验现象 | 实验结论 |
原因: | 猜想的结论正确 |
(4)化学反应可控制才能更好地为人类造福,我们可以通过改变反应的条件、药品用量、改进装置等途径来达到控制反应的目的。常温下块状电石(CaC2)与水反应生成乙炔 (C2H2)气体和氢氧化钙,该反应的化学方程式是 , 实验室制取乙炔时,须严格控制加水速度,以免剧烈反应放热引起装置炸裂.图中适合制取乙炔气体的发生装置有(填装置序号)。
【答案】
(1)长颈漏斗,水槽
(2)AF或AH,试管口没有棉花团,2KMnO4 ![]() K2MnO4+MnO2+O2↑,②③
K2MnO4+MnO2+O2↑,②③
(3)石灰水已经完全变质,滴加几滴无色酚酞试液,振荡,观察到溶液变红色,说明石灰水没有变质(或原因二:气体中有挥发出来的HCl气体;取少量加有稀硝酸的硝酸银溶液于试管中,然后将生成的气体通入试管中,产生白色沉淀,说明气体中有HCl气体)
(4)CaC2+2H2O=C2H2↑+Ca(OH)2,D
【解析】解:(1)根据实验室常用仪器可知:a长颈漏斗;c水槽;(2)如果用高锰酸钾制氧气就需要加热,故发生装置选A,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,化学方程式为:2KMnO4 ![]() K2MnO4+MnO2+O2↑;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,向上排空气法收集的氧气比较干燥;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;(3)某同学取一定浓度盐酸与石灰石反应,将生成的气体通入澄清石灰水中,始终未见浑浊,可能原因一:石灰水已经完全变质;滴加几滴无色酚酞试液,振荡,观察到溶液变不红色,说明石灰水完全变质;原因二:气体中有挥发出来的HCl气体;取少量加有稀硝酸的硝酸银溶液于试管中,然后将生成的气体通入试管中,产生白色沉淀,说明气体中有HCl气体;(4)据制取乙炔气体,是在常温下用块状电石与水反应,即固体和液体的反应;又因为该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂,所以应选用装置D。D装置加液体的是注射器,可控制加水的速度。该反应的化学方程式是CaC2+2H2O=C2H2↑+Ca(OH)2。
K2MnO4+MnO2+O2↑;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,向上排空气法收集的氧气比较干燥;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;(3)某同学取一定浓度盐酸与石灰石反应,将生成的气体通入澄清石灰水中,始终未见浑浊,可能原因一:石灰水已经完全变质;滴加几滴无色酚酞试液,振荡,观察到溶液变不红色,说明石灰水完全变质;原因二:气体中有挥发出来的HCl气体;取少量加有稀硝酸的硝酸银溶液于试管中,然后将生成的气体通入试管中,产生白色沉淀,说明气体中有HCl气体;(4)据制取乙炔气体,是在常温下用块状电石与水反应,即固体和液体的反应;又因为该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂,所以应选用装置D。D装置加液体的是注射器,可控制加水的速度。该反应的化学方程式是CaC2+2H2O=C2H2↑+Ca(OH)2。
所以答案是:(1)长颈漏斗;水槽;(2)AF或AH;试管口没有棉花团;2KMnO4 ![]() K2MnO4+MnO2+O2↑;②③;(3)石灰水已经完全变质;滴加几滴无色酚酞试液,振荡;观察到溶液变红色,说明石灰水没有变质(或原因二:气体中有挥发出来的HCl气体;取少量加有稀硝酸的硝酸银溶液于试管中,然后将生成的气体通入试管中,产生白色沉淀,说明气体中有HCl气体);(4)CaC2+2H2O=C2H2↑+Ca(OH)2;D。
K2MnO4+MnO2+O2↑;②③;(3)石灰水已经完全变质;滴加几滴无色酚酞试液,振荡;观察到溶液变红色,说明石灰水没有变质(或原因二:气体中有挥发出来的HCl气体;取少量加有稀硝酸的硝酸银溶液于试管中,然后将生成的气体通入试管中,产生白色沉淀,说明气体中有HCl气体);(4)CaC2+2H2O=C2H2↑+Ca(OH)2;D。
【考点精析】本题主要考查了书写化学方程式、文字表达式、电离方程式的相关知识点,需要掌握注意:a、配平 b、条件 c、箭号才能正确解答此题.

【题目】某校化学兴趣小组的同学测定了来自三个不同地方的铜和硫的化合物样品,实验数据如下:
样品 | 样品质量/g | 铜元素的质量/g | 硫元素的质量/g |
1 | 5.02 | 3.35 | 1.67 |
2 | 10.05 | 6.71 | 3.34 |
3 | 99.6 | 66.4 | 33.2 |
根据表中数据,你能得出的结论是( )
A.样品1中铜元素的质量分数为50%
B.样品2的化合物的化学式是Cu2S
C.样品3中铜元素与硫元素的质量比为2:1
D.三个不同地方样品可能属于同一种物质