题目内容
【题目】(12分) 结合下列实验装置回答相关问题:
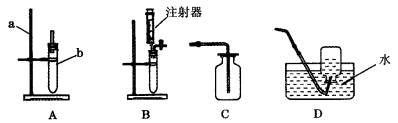
(1)实验室用石灰石与稀盐酸反应制CO2的化学方程式为:____________,收集装置应选________(填编号);
实验室用双氧水制O2的化学方程式为:_________________________________。
(2)若用B作制气装置,与A相比,其优点是_________________________(写一点)。
(3)用KClO3和MnO2制O2,若选用A作发生装置,则还要增加_________________(填仪器名称),并把A作如下改动:____________________________。发生反应的化学方程式为: ___________________。
【答案】(1) CaCO3 + 2HCl = CaCl2 + CO2↑+ H2O(2分) C(1分)
2H2O2![]() 2H2O + O2↑(2分)
2H2O + O2↑(2分)
(2) 方便加液体(或可控制液体滴加速度,控制化学反应速率)(2分)
(3) 酒精灯(1分) 将试管口略向下倾斜(2分)
2KClO3![]() 2KCl + 3O2↑(
2KCl + 3O2↑(
【解析】
试题分析:(1)实验室用石灰石与稀盐酸反应制取二氧化碳的同时还生成了氯化钙和水:
CaCO3 + 2HCl = CaCl2 + CO2↑+ H2O;二氧化碳的密度比空气大,易溶于水,故只能用向上排空气法收集,选C装置;过氧化氢在二氧化锰的催化作用下分解生成水和氧气:2H2O2![]() 2H2O + O2↑;
2H2O + O2↑;
(2)根据题意,固体和液体接触后,反应便立即开始,不能人为控制其速率和生成的气体的量,故要控制其反应速率,可通过控制液体药品的加入量来实现;注射器就可以控制加入液体药品的量和速率;
(3)用KClO3和MnO2制O2,根据反应物的状态和反应条件选择发生装置,应选固固加热型,故还需要酒精灯;氯酸钾分解生成氯化钾和氧气:2KClO3![]() 2KCl + 3O2↑。
2KCl + 3O2↑。

【题目】石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:
次数 | 第1次 | 第2次 | 第3次 |
加入盐酸的质量/g | 10 | 10 | 10 |
剩余固体的质量/g | 16 | 12 | 8 |
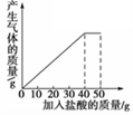
请计算:
(1)石灰石样品中杂质的质量为 g。
(2)所加盐酸的溶质质量分数.