题目内容
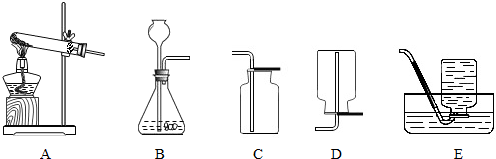
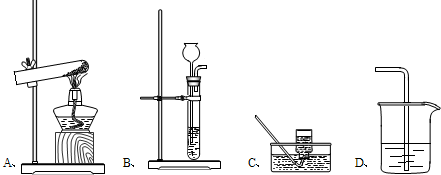
今有A、B、C、D、E、F、G七种实验装置(如下图所示)请按要求回答下列问题:
(1)实验室用石灰石和稀盐酸制取二氧化碳时,应选择的气体发生和收集装置是
(2)若要收集到不含HCl且干燥的二氧化碳,应选择的净化和收集装置是
(3)AgNO3溶液的作用是除掉二氧化碳中混有的少量氯化氢气体,反应的化学方程式为:
(4)若将B装置中的药品换成双氧水和二氧化锰,则B装置中的化学反应方程式为:

(1)实验室用石灰石和稀盐酸制取二氧化碳时,应选择的气体发生和收集装置是
BC
BC
,反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑
CaCO3+2HCl═CaCl2+H2O+CO2↑
;(2)若要收集到不含HCl且干燥的二氧化碳,应选择的净化和收集装置是
F
F
(3)AgNO3溶液的作用是除掉二氧化碳中混有的少量氯化氢气体,反应的化学方程式为:
HCl+AgNO3=AgCl↓+HNO3
HCl+AgNO3=AgCl↓+HNO3
.AgNO3溶液不能换成石灰水,理由是二氧化碳能与石灰水反应
二氧化碳能与石灰水反应
.浓硫酸的作用是干燥二氧化碳气体
干燥二氧化碳气体
(4)若将B装置中的药品换成双氧水和二氧化锰,则B装置中的化学反应方程式为:
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
分析:(1)根据实验室制取二氧化碳的反应物的状态和反应的条件确定发生装置,根据气体的收集方法确定收集装置,根据反应原理写出反应的方程式;
(2)根据给出的装置,可用硝酸银溶液吸收氯化氢气体,用浓硫酸干燥气体;
(3)硝酸银溶液与氯化氢反应生成了氯化银沉淀和硝酸,写出反应的方程式,根据二氧化碳与石灰水的反应分析AgNO3溶液不能换成石灰水的理由,浓硫酸具有吸水性,可用作干燥剂;
(4)根据双氧水制取氧气的反应写出反应的方程式.
(2)根据给出的装置,可用硝酸银溶液吸收氯化氢气体,用浓硫酸干燥气体;
(3)硝酸银溶液与氯化氢反应生成了氯化银沉淀和硝酸,写出反应的方程式,根据二氧化碳与石灰水的反应分析AgNO3溶液不能换成石灰水的理由,浓硫酸具有吸水性,可用作干燥剂;
(4)根据双氧水制取氧气的反应写出反应的方程式.
解答:解:(1)实验室用大理石和稀盐酸反应制取二氧化碳,反应物的状是固体和液体,反应条件是常温,应选用发生装置B,由于二氧化碳的密度大于空气的密度,可选用收集装置C,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)若要收集到不含HCl且干燥的二氧化碳,可用硝酸银溶液吸收氯化氢气体,用浓硫酸干燥气体,应选择的净化和收集装置是F;
(3)硝酸银溶液与氯化氢反应生成了氯化银沉淀和硝酸,反应的方程式是:HCl+AgNO3=AgCl↓+HNO3,由于据二氧化碳与石灰水的反应,所以AgNO3溶液不能换成石灰水.浓硫酸具有吸水性,可用作干燥二氧化碳气体;
(4)双氧水在二氧化锰的催化作用下分解生成了氧气,反应的方程式是:2H2O2
2H2O+O2↑.
故答为:(1)BC,CaCO3+2HCl═CaCl2+H2O+CO2↑;(2)F;(3)HCl+AgNO3=AgCl↓+HNO3,二氧化碳与石灰水的反应,干燥二氧化碳气体(4)2H2O2
2H2O+O2↑.
(2)若要收集到不含HCl且干燥的二氧化碳,可用硝酸银溶液吸收氯化氢气体,用浓硫酸干燥气体,应选择的净化和收集装置是F;
(3)硝酸银溶液与氯化氢反应生成了氯化银沉淀和硝酸,反应的方程式是:HCl+AgNO3=AgCl↓+HNO3,由于据二氧化碳与石灰水的反应,所以AgNO3溶液不能换成石灰水.浓硫酸具有吸水性,可用作干燥二氧化碳气体;
(4)双氧水在二氧化锰的催化作用下分解生成了氧气,反应的方程式是:2H2O2
| ||
故答为:(1)BC,CaCO3+2HCl═CaCl2+H2O+CO2↑;(2)F;(3)HCl+AgNO3=AgCl↓+HNO3,二氧化碳与石灰水的反应,干燥二氧化碳气体(4)2H2O2
| ||
点评:气体的实验室制法主要从反应原理、发生装置、收集装置、检验、验满及实验操作注意事项等方面进行比较、归纳,总结实验室制取气体的一般思路和方法.

练习册系列答案
相关题目