题目内容
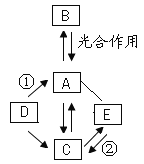
【题目】我国有丰富的钛铁矿资源,钛铁矿的主要成分是钛酸亚铁(FeTiO3),利用钛铁矿可以提取金属钛。以下为某化工企业从钛铁矿中提取金属钛的流程示意图,请回答下列问题:
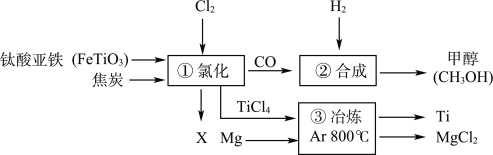
(1)钛酸亚铁(FeTiO3)中钛元素的化合价为________价。
(2)①中反应为2FeTiO3+6C+7Cl2![]() 2X+2TiCl4+6CO,则X为____,该反应______(填“是”或“否”)属于置换反应。
2X+2TiCl4+6CO,则X为____,该反应______(填“是”或“否”)属于置换反应。
(3)②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为__________。
(4)③中发生反应的化学方程式为___________,该反应中Ar的作用是____________。
【答案】+4 FeCl3 否 7∶1 2Mg+TiCl4![]() Ti+2MgCl2 作保护气
Ti+2MgCl2 作保护气
【解析】
(1)根据在化合物中正负化合价代数和为零考虑;
(2)根据质量守恒定律推断x的化学式;
(3)根据氢气和一氧化碳反应的方程式考虑质量比;
(4)根据化学方程式的书写方法写化学方程式。
(1)设FeTiO3中P的化合价是x,FeTiO3中Fe的化合价是+2价,O的化合价是-2价,利用化合物中各元素的化合价的代数和为零的原则得到方程(+2)+x+(-2)×3=0,解得,x=+4 所以钛酸亚铁(FeTiO3)中钛元素的化合价是+4价;
(2)根据质量守恒定律,在反应前后各元素原子的个数不变;从2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO看钛原子、氧原子、碳原子反应前后除物质x外个数已经相等,故x中无钛原子、氧原子、碳原子.铁反应前共有2个,反应后只有x有,所以2x中有2个,从而x中有1个;氯原子反应前有14个,反应后x除外有8个,所以2x中有6个,因此x中有3个,因此x的化学式是FeCl3;
(3)根据从化学方程式
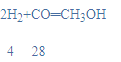
由此可知一氧化碳和氢气的质量比是:28:4=7:1;
(4)TiCl4与Mg反应的反应物是TiCl4与Mg,生成物是Ti和MgCl2,用观察法配平即可,因此该反应的化学方程式是TiCl4+2Mg![]() Ti+2MgCl2,该反应中Ar的作用是作保护气。
Ti+2MgCl2,该反应中Ar的作用是作保护气。