��Ŀ����
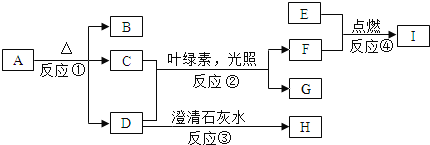
����Ŀ��ij�о���ѧϰС��Ϊ̽��þ��ˮ�ķ�Ӧ���������ʵ�飺
����1����þ����ɰֽ��ĥ���������ֳ����ȷݣ�
����2����һ�ݹ�����þ��������ˮ�У�����û�й۲쵽�κ�����
����3������һ�ݹ�����þ��������ˮ�У��۲쵽�����ݲ�����
���������ϡ����ٷ�̪��Һ�����������NaOH��Mg��OH��2�����ñ�죻
�ڻ��ý�������Na����ˮ�����û���Ӧ�����������������������Խ���ã����ɵ������������Խǿ��
��1����þ����ɰֽ��ĥ��������ԭ���� ��
��2��ͬѧ������3���ձ��еμӷ�̪��Һ���۲쵽þ���ı��������Եĺ�ɫ���֣��÷�Ӧ�Ļ�ѧ����ʽΪ ��
��3������2��3�Աȿ�֪��Ӱ��þ��ˮ�ķ�Ӧ���ʵ�һ�������� ��
��4���������Ƽӵ�����ͭ��Һ�У�δ���ֺ�ɫ��������������������Ϣ������Ϊ���ܹ۲쵽�������� ��
���𰸡���1����ȥ���������Ĥ��
��2��Mg+2H2O![]() Mg��OH��2+H2������3���¶ȣ�
Mg��OH��2+H2������3���¶ȣ�
��4���������������Һ�в�����ɫ������
����������1������þ�ܱ������е�����������������þ�����Խ�þ����ɰֽ��ĥ��������ԭ���ǣ���ȥ���������Ĥ�������ȥ���������Ĥ��
��2��þ������ˮ��Ӧ����������þ���������÷�Ӧ�Ļ�ѧ����ʽΪMg+2H2O![]() Mg��OH��2+H2�����÷�Ӧ��һ�ֵ��ʺͻ����ﷴӦ��������ĵ��ʺͻ���������û���Ӧ�����Mg+2H2O
Mg��OH��2+H2�����÷�Ӧ��һ�ֵ��ʺͻ����ﷴӦ��������ĵ��ʺͻ���������û���Ӧ�����Mg+2H2O![]() Mg��OH��2+H2����
Mg��OH��2+H2����
��3�����ݲ���2��3�Աȿ�֪�����ߵIJ�֮ͬ�������¶Ȳ�ͬ�����Բ���2��3�Աȿ�֪��Ӱ��þ��ˮ��Ӧ���ʵ��������¶ȣ�����¶ȣ�
��4�������ƵĻ�Դ��ڽ���þ�����Խ������Ƽӵ�����ͭ��Һ�У�������Ҫ����ˮ��Ӧ�����������ƺ�����������������Һ������ͭ��Һ��Ӧ����������ͭ��ɫ�����������ƣ������������Ƽӵ�����ͭ��Һ�У��Ʋ���ܹ۲쵽���������������������Һ�в�����ɫ����������������������Һ�в�����ɫ������

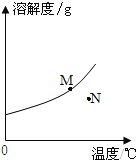
����Ŀ��NaNO3��KNO3���ܽ�����ݼ��ܽ���������£�����˵����ȷ���ǣ� ��

�¶�/�� | 20 | 30 | 50 | 60 | 80 | |
�ܽ��S/g | NaNO3 | 87.6 | 94.9 | 110 | 122 | 148 |
KNO3 | 31.6 | 45.3 | 85.5 | 110 | 167 |
A��30��ʱ��������Һ����������������NaNO3��KNO3
B���ұ�ʾKNO3�ܽ������
C��t1��ʱNaNO3��KNO3���ܽ����ȣ���ʱ�¶�Ϊ60��80��֮��
D����Ӱ��NaNO3��KNO3����Һ��Ϊ������Һ