题目内容
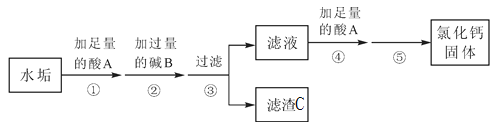
【题目】硬水受热后会产生水垢,水垢的主要成分是CaCO3和Mg(OH)2,其它成分不参与反应。.实验室由水垢制取纯净CaCl2固体的流程如下:
请按要求填空:
(1)酸A的化学式是__________;碱B的化学式是________________;
(2)步骤④加酸A的作用是______________;
(3)步骤⑤是利用____________的方法得到氯化钙固体。
(4)用滤渣C经两步化学反应可制得其中所含金属元素的单质,写出两步化学反应的化学方程式:_________,__________。
【答案】 HCl Ca(OH)2 除去过量的氢氧化钙(或中和过量的氢氧化钙) 蒸发溶剂(或蒸发结晶) Mg(OH)2 + 2HCl == MgCl2 + 2H2O MgCl2![]() Mg + Cl2↑
Mg + Cl2↑
【解析】主要考查了酸、碱的有关的化学性质及有关的化学方程式的书写。读懂流程图,根据酸、碱的性质进行分析。
(1)根据流程图,滤液加入足量的酸A生成了氯化钙,所以酸A是盐酸,化学式为:HCl;步骤①中加入盐酸,CaCO3和Mg(OH)2转化为CaCl2和MgCl2,步骤②中加入过量碱是为了除去MgCl2,为了不引入杂质,加入的碱应为氢氧化钙,化学式Ca(OH)2;
(2)步骤②加入的是过量的氢氧化钙,最后要得到氯化钙,需要将氢氧化钙除去,所以步骤④加酸A的作用除去过量的氢氧化钙( 或中和过量的氢氧化钙);
(3)步骤⑤是利用蒸发溶剂(或蒸发结晶)的方法得到氯化钙固体;
(4)滤渣C是氢氧化钙与氯化镁反应生成的氢氧化镁,氢氧化镁先与盐酸反应生成氯化镁和水,再将氯化镁通电分解生成可得到金属镁,化学方程式分别是:Mg(OH)2 + 2HCl == MgCl2 + 2H2O;MgCl2![]() Mg + Cl2↑。
Mg + Cl2↑。

【题目】(6分)下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
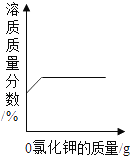
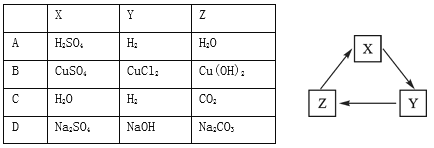
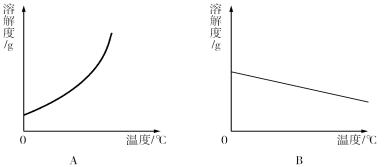
(1)依据上表数据,绘制了Ca(OH)2和NaOH的溶解度曲线,下图中能表示NaOH溶度曲线的是 (填“A”或“B”);
(2)将一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙 ②升高温度 ③降低温度 ④加入水 ⑤蒸发水后再恢复到原温度 ⑥加入生石灰。
其中措施正确的是 ;
A.②④⑥ B.③④ C.①③⑤⑥ D.①②⑤⑥
(3)20℃时,191g饱和NaOH溶液,蒸发10g水后,再恢复到20℃,可析出NaOH固体的质量为 ;
(4)现有20℃时Ca(OH)2的饱和溶液甲,向其中加入一定量CaO后得到溶液乙,此时溶液中溶质的质量
乙 甲(填“>”、“<”或“=”);
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH固体,应采取的物理方法是 ;
(6)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH (填“偏大”、“偏小”或“不受影响”)。
【题目】化学活动小组围绕磷燃烧的化学反应,展开了如下探究活动:
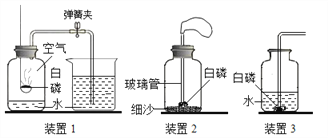
(1)空气中氧气含量的测定
① 表1实验记录
实验目的 | 空气中氧气含量的测量 |
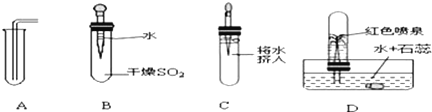
实验装置 | 见装置1 |
现象(证据) | |
实验结论 | 氧气约占空气总体积的五分之一 |
则上表1中的“现象(证据)”栏目应填___________(可多选)。
A. 产生白雾 B. 放出热量 C. 产生五氧化二磷 D. 瓶内水面上升约1/5
② 同学们对该实验进行交流,你认为正确的是___________(可多选)
A. 改用放大镜聚光引燃会更合理
B. 铁丝燃烧产生固体Fe304,用铁丝代替白磷也能达到实验目的
C. 白磷(过量)燃烧熄灭后剩余气体主要是氮气,由此可看出氮气不燃烧,也不支持燃烧
D. 白磷燃烧结束后不能立即打开弹簧夹的原因是怕冷水进入集气瓶使集气瓶破裂
(2)验证质量守恒定律
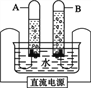
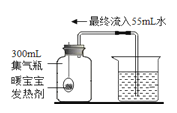
①乙同学将装置1改装为装置2,为了验证质量守恒定律还需要的仪器是___________。
②调节仪器,称量整个装置的初始质量![]() ,将胶塞上的玻璃管在酒精灯上灼烧,迅速塞紧瓶塞,重新把装置进行称量,质量为
,将胶塞上的玻璃管在酒精灯上灼烧,迅速塞紧瓶塞,重新把装置进行称量,质量为![]() (不考虑气球带来的浮力)。实验结束之后,发现反应后质量减少(
(不考虑气球带来的浮力)。实验结束之后,发现反应后质量减少(![]() ),同学们分析原因如下,你认为正确的是___________(可多选)
),同学们分析原因如下,你认为正确的是___________(可多选)
A. 装置漏气 B. 白磷量不足 C. 气球破损 D. 没冷却到室温就称量
(3)燃烧条件的探究
丙同学用装置3进行燃烧条件的探究(白磷的着火点为40℃)设计了如下实验:
① 实验记录
实验序号 | Ⅰ | Ⅱ | Ⅲ |
实验操作 | 将白磷浸入40℃的热水 | 将白磷浸入40℃的热水,通入氧气 | 将白磷浸入冷水 中,通入氧气 |
实验现象 | 白磷不燃烧 | 白磷燃烧 | _______________ |
② 实验分析:对比_________和__________(填实验序号“Ⅰ”“Ⅱ”“Ⅲ”),可知可燃烧物燃烧的条件是温度达到着火点。
(4)探究活动(1)(2)(3)中共同的反应的化学方程式是________________________。