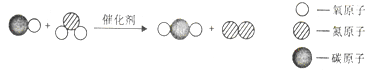题目内容
【题目】在反应2A+5B═2C+4D中,C﹑D的相对分子质量之比为9:22,若2.6g A与B完全反应后,生成8.8g D.则在此反应中B与D的质量比为
A.4:9 B.8:1 C.10:11 D.31:44
【答案】C
【解析】试题分析: 假设C的相对分子质量为9,D的相对分子质量为22,根据质量守恒定律进行计算。假设生成C的质量为X
2A+5B=2C+4D
18 88
X 8.8g
18/88=X/8.8g X=1.8g 则参加反应B的质量="8.8g+1.8g-2.6" g =8g
则此反应中B与D的质量比=8g:8.8g=10:11
故选C

 轻松暑假总复习系列答案
轻松暑假总复习系列答案【题目】过碳酸钠(化学式为2Na2CO33H2O2)俗名固体双氧水。溶于水可看作是Na2CO3溶液和H2O2溶液混合。为了方便保存,过碳酸钠样品可能添加少量的MgSO4和硅酸镁中的一种或二种作为稳定剂。已知①双氧水可用于供氧、消毒和漂白;②硅酸镁不溶于水。
(1)过碳酸钠的用途不合理的是 。
A.鱼池供氧剂 B.消毒剂 C.干燥剂 D.漂白剂
(2)取少量过碳酸钠样品于烧杯中,加入足量蒸馏水,有不溶于水的固体产生。判断样品中 有硅酸镁。(填写“可能”或“一定”)
(3)利用实验室限选试剂,设计实验确定该样品中是否添加少量的MgSO4。
限选试剂:稀盐酸、稀H2SO4、BaCl2溶液、蒸馏水、AgN03溶液
实验操作 | 预期现象和必要结论 |
步骤:1:取少量样品于烧杯中,缓慢加入足量蒸馏水,充分搅拌,静置,过滤。 |
|
步骤2:取少量步骤1所得的滤液于试管中,加入 ,振荡后静置。 | |
步骤3:取少量步骤2所得的溶液于试管中, 。 | ,说明样品中有MgSO4。 ,说明样品中没有MgSO4。 |
【题目】甲、乙、丙是初中化学常见物质。这些物质之间的转化关系如下图所示。
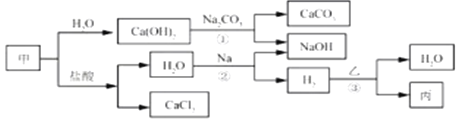
根据以上信息,请回答下列问题。
(1)写出甲的化学式__________。
(2)写出反应①的化学方程式_______________。
(3)写出反应②的化学方程式_______________。该反应属于_____反应(填基本反应类型)。
(4)反应③在一定温度下进行,若乙为Fe2O3,则丙为Fe;若丙为Cu,则乙为_______(填化学式)。
(5)请完成下列表格,证明Fe的金属活动性比Cu的强。
实验方案 | 实验现象 |
将铁片浸入_______(填化学式)溶液中 | 铁片表明析出______固体 |
【题目】下表中除去物质中少量杂质的方法错误的是
选项 | 物质 | 所含杂质 | 除去杂质的方法 |
A | 铜粉 | 铁粉 | 用磁铁吸引 |
B | 二氧化碳 | 氯化氢 | 通过足量的氢氧化钠溶液 |
C | 硫酸钠溶液 | 碳酸钠 | 加入适量稀硫酸 |
D | 碳酸钙 | 氯化钙 | 加适量的水溶解、过滤、洗涤、干燥 |
A. A B. B C. C D. D