题目内容
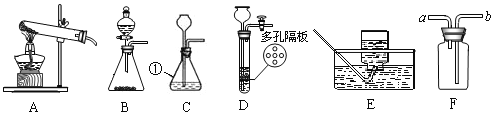
【题目】进行如下图所示微型实验,研究物质的性质。
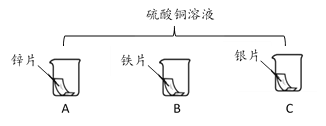
(1)能发生反应的是_______(填字母序号)。
(2)若要验证铁、铜、银的金属活动性顺序,依据的现象是____,反应的化学方程式为_____。
(3)在锌、铁、铜、银中,通过该实验,无法比较金属活动性顺序的两种金属是______。
【答案】AB B中铁片表面有红色固体析出,溶液由蓝色逐渐变为浅绿色,C中无明显现象 Fe+CuSO4=FeSO4+Cu 锌、铁
【解析】
(1)排在金属活动性顺序前面的金属能将排在后面的金属从其盐溶液中置换出来,锌、铁的活动性比铜强,锌、铁都能和硫酸铜反应置换出铜,银的活动性比铜弱,银不能置换出硫酸铜中的铜,故填AB;
(2)铁比铜活泼,能置换出硫酸铜中的铜,反应现象是铁表面有红色固体析出,溶液由蓝色逐渐变为浅绿色,银的活动性比铜弱,不能置换出硫酸铜中的铜,反应时无明显现象,依据故填B中铁片表面有红色固体析出,溶液由蓝色逐渐变为浅绿色,C中无明显现象;铁和硫酸铜反应生成硫酸亚铁和铜,方程式故填Fe+CuSO4=FeSO4+Cu;
(3)锌、铁都能置换出硫酸铜中的铜,即锌、铁都比铜活泼,但无法比较锌铁的活动性强弱,故填锌、铁。

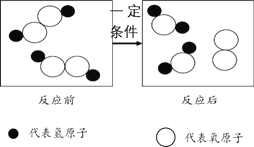
【题目】物质都是由微观粒子构成的。在构成下列四种物质的微粒示意图中, “○”和“● ”分别表示氢和氧两种元素的原子。
物质 | 甲 | 乙 | 丙 | 丁 |
构成该物质的粒子 |
|
|
|
|
(1)乙物质的一个分子中含有_________ 个原子。
(2)四种物质中,属于单质的是___________ (填物质代号,下同)。
(3)四种物质中,不同种元素原子个数比为 1:1 的是_________ ,含有![]() 分子的是________ 。
分子的是________ 。
(4)甲物质在一定条件下反应可生成丙,该反应的化学方程式为_____________ , 该反应属于________ 反应(填“化合”或“分解”)。
【题目】下列实验方案合理的是![]()
![]()
实验目的 | 所用试剂或方法 | |
A | 除去CO中混有 | 通入氧气点燃 |
B | 量取 | 用100mL的量筒 |
C | 验证锌、铜、银的金属活动性 | 加稀盐酸 |
D | 除去 | 加过量的铜粉,过滤 |
A. A B. B C. C D. D