题目内容
【题目】碳及其氧化物性质的应用。
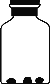
(1)如图所示,向盛有红棕色二氧化氮气体的集气瓶里投入几小块烘烤过的木炭,红棕色消失,说明木炭具有_____能力,其原因是木炭具有_____的结构。
(2)在书写具有保存价值的档案时,规定应使用碳素墨水,原因是_____
(3)将一定质量的金刚石在足量的氧气中充分燃烧,固体全部消失,写出反应的化学方程式:_____;将生成的产物用足量的氢氧化钠溶液来充分吸收并测定其质量,当金刚石的质量恰好等于_____时,则可证明金刚石是由碳元素组成的单质。
(4)在实验室里,检验二氧化碳一般用澄清石灰水,而吸收二氧化碳常用氢氧化钠溶液,理由是_____。
【答案】吸附 疏松多孔 常温下,碳的化学性质稳定 C+O2![]() CO2 氢氧化钠吸收的二氧化碳中的碳元素 二氧化碳和澄清石灰水反应现象明显,但氢氧化钠在水中的溶解性比氢氧化钙大,吸收二氧化碳的能力强
CO2 氢氧化钠吸收的二氧化碳中的碳元素 二氧化碳和澄清石灰水反应现象明显,但氢氧化钠在水中的溶解性比氢氧化钙大,吸收二氧化碳的能力强
【解析】
(1)向盛有红棕色二氧化氮气体的集气瓶里投入几小块烘烤过的木炭,红棕色消失,说明木炭具有 吸附能力,其原因是木炭具有疏松多孔的结构;
(2)在书写具有保存价值的档案时,规定应使用碳素墨水,因为需要长期保存,说明碳的性质稳定,具体描述为碳素墨水中含有碳,在常温下,碳的化学性质不活泼;
(3)将一定质量的金刚石在足量的氧气中充分燃烧,固体全部消失,写出反应的化学方程式 C+O2![]() CO2 ;将生成的产物用足量的氢氧化钠溶液来充分吸收并测定其质量,当金刚石的质量恰好等于生成的二氧化碳中碳元素的质量时,则可证明金刚石是由碳元素组成的单质;
CO2 ;将生成的产物用足量的氢氧化钠溶液来充分吸收并测定其质量,当金刚石的质量恰好等于生成的二氧化碳中碳元素的质量时,则可证明金刚石是由碳元素组成的单质;
(4)在实验室里,检验二氧化碳一般用澄清石灰水,而吸收二氧化碳常用氢氧化钠溶液,理由是澄清石灰水、氢氧化钠溶液分别与二氧化碳反应的现象不同;氢氧化钠、氢氧化钙溶解性的大小,氢氧化钠溶液和氢氧化钙溶液分别吸收二氧化碳的能力不同。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案