题目内容
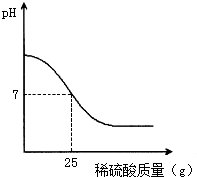 向50g溶质质量分数为4%的氢氧化钠溶液中逐滴加入一定质量分数的稀硫酸,所滴加的稀硫酸质量与溶液的pH变化的函数关系如图所示,稀硫酸溶质的质量分数为( )
向50g溶质质量分数为4%的氢氧化钠溶液中逐滴加入一定质量分数的稀硫酸,所滴加的稀硫酸质量与溶液的pH变化的函数关系如图所示,稀硫酸溶质的质量分数为( )| A、4% | B、4.9% | C、9.8% | D、19.6% |
分析:由所滴加的稀硫酸质量与溶液的pH变化的函数关系图,在加入25g稀硫酸所得溶液pH=7时,硫酸与氢氧化钠恰好反应;根据反应的化学方程式,由消耗氢氧化钠的质量计算所加稀硫酸中硫酸的质量,由溶质质量分数计算公式求出稀硫酸溶质的质量分数.
解答:解:由关系图,加入25g稀硫酸所得溶液pH=7时,硫酸与氢氧化钠恰好反应;
设稀硫酸溶质的质量分数为x
H2SO4 +2NaOH═Na2SO4+2H2O
98 80
25g×x 50g×4%
=
x=9.8%
故选C.
设稀硫酸溶质的质量分数为x
H2SO4 +2NaOH═Na2SO4+2H2O
98 80
25g×x 50g×4%
| 98 |
| 25g×x |
| 80 |
| 50g×4% |
x=9.8%
故选C.
点评:在使用化学方程式进行计算时,所使用的需为纯净物的质量,不能直接把溶液的质量代入化学方程式进行计算.

练习册系列答案
相关题目
 (2006?顺义区二模)向50g溶质质量分数为10%的氢氧化钠溶液中逐滴加入一定质量分数的稀硫酸,所加稀硫酸的质量与溶液pH变化的关系如图所示,根据曲线计算:
(2006?顺义区二模)向50g溶质质量分数为10%的氢氧化钠溶液中逐滴加入一定质量分数的稀硫酸,所加稀硫酸的质量与溶液pH变化的关系如图所示,根据曲线计算: N2↑+Cl2↑+2O2↑+4X.X的化学式为______.
N2↑+Cl2↑+2O2↑+4X.X的化学式为______.