题目内容
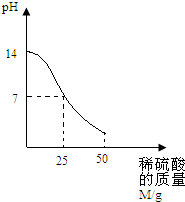 (2006?顺义区二模)向50g溶质质量分数为10%的氢氧化钠溶液中逐滴加入一定质量分数的稀硫酸,所加稀硫酸的质量与溶液pH变化的关系如图所示,根据曲线计算:
(2006?顺义区二模)向50g溶质质量分数为10%的氢氧化钠溶液中逐滴加入一定质量分数的稀硫酸,所加稀硫酸的质量与溶液pH变化的关系如图所示,根据曲线计算:(1)所加稀硫酸溶液中溶质的质量分数.
(2)实验结束,所得溶液中硫酸钠的质量分数.
分析:观察图示,由所滴加的稀硫酸质量与溶液的pH变化的函数关系图,在加入25g稀硫酸所得溶液pH=7时,硫酸与氢氧化钠恰好反应;根据反应的化学方程式,由消耗氢氧化钠的质量计算所加稀硫酸中硫酸的质量,生成的硫酸钠的质量,由溶质质量分数计算公式求出稀硫酸溶质的质量分数和所得溶液中硫酸钠的质量分数.
解答:解:设恰好完全反应时消耗的硫酸溶液中含有溶质的质量为x,反应生成硫酸钠的质量为y
2NaOH+H2SO4=Na2SO4+2H2O
80 98 142
50g×10% x y
=
x=6.125g
=
y=8.875g
所加稀硫酸溶液中溶质的质量分数为:
×100%=24.5%
所得溶液中硫酸钠的质量分数为;
×100%=11.8%
答:(1)所加稀硫酸溶液中溶质的质量分数是24.5%;(2)实验结束,所得溶液中硫酸钠的质量分数是11.8%.
2NaOH+H2SO4=Na2SO4+2H2O
80 98 142
50g×10% x y
| 80 |
| 98 |
| 50g×10% |
| x |
| 80 |
| 142 |
| 50g×10% |
| y |
所加稀硫酸溶液中溶质的质量分数为:
| 6.125g |
| 25g |
所得溶液中硫酸钠的质量分数为;
| 8.875g |
| 50g+25g |
答:(1)所加稀硫酸溶液中溶质的质量分数是24.5%;(2)实验结束,所得溶液中硫酸钠的质量分数是11.8%.
点评:此题是一道结合图象的计算题,解题时找到PH=7的恰好反应点,并利用化学方程式的计算进行解决是解题的突破口.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目