题目内容
【题目】在探究某破损的试剂瓶内的氢氧化钠是否变质的问题时,4个小组的实验数据如下:
第一组 | 第二组 | 第三组 | 第四组 | |
取用样品的质量 | 10g | 10g | 10g | 10g |
加入氯化钙溶液的体积 | 10ml | 20ml | 30ml | 40ml |
得到沉淀的质量 | 2.0g | 4.0g | 5.0g | 5.0g |
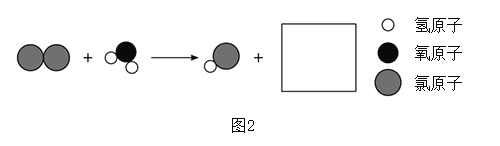
(1)氢氧化钠在空气中变质的原因可用化学方程式表示为__________;
(2)根据实验数据分析,该试剂瓶内氢氧化钠的变质情况是下列中的__________;
A没有变质 B部分变质 C完全变质
(3)根据上述实验数据,欲通过实验将该试剂瓶内的200g药品中的杂质除去,制得纯净的氢氧化钠:
①需要氢氧化钙的质量为______g;
②具体的实验操作是将药品全部溶解、加入称量好的氢氧化钙并搅拌、_______、蒸发结晶。
【答案】![]() B 74 过滤
B 74 过滤
【解析】
(1)氢氧化钠在空气中变质,是因为氢氧化钠和二氧化碳反应生成碳酸钠和水,化学方程式表示为:![]() 。
。
(2)设样品中碳酸钠质量为x,
根据实验数据分析可知,最终生成碳酸钙质量是5.0g,

![]()
x=5.3g,
该试剂瓶内氢氧化钠质量:10g-5.3g=4.7g,因此氢氧化钠部分变质。
(3)10g该样品中,5.3g碳酸钠,故该试剂瓶内的200g药品中碳酸钠的质量为5.3×20=106g;
①设需要氢氧化钙的质量为y,
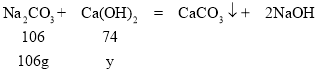
![]()
y=74g
需要氢氧化钙的质量为74g。
②具体的实验操作是将药品全部溶解、加入称量好的氢氧化钙、过滤、蒸发结晶。

 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案【题目】同学们在学习了氧气的制取和性质后,对课后习题中所提供的仪器、药品产生了浓厚的兴趣,利用它们及其他必要物品进行实验并展开探究。

(1)小丽选择了上述仪器中的__________(填字母序号,下同)组装了制取氧气的发生装置,反应的文字表达式为__________。为了收集到纯净的氧气,她选择的仪器是_____________。
(2)同学们又对提供的红砖粉末进行探究。
[提出问题]红砖粉末能否作为过氧化氢溶液分解的催化剂?它是否比二氧化锰的催化效果更好?
[实验探究]
实验步骤 | 实验操作及现象 | 实验结论 |
步骤一 | 取5 mL过氧化氢溶液于试管中,将带火星的木条伸入试管中,木条没有复燃;向上述试管中加人少量红砖粉末,将带火星木条伸入试管中,木条复燃。 | _____________。 |
步骤二 | 在步骤一的试管中再次加人过氧化氢溶液,将带火星木条伸入试管中,木条复燃,待试管中又没有现象发生时,再多次重复上述操作,看到带火星木条依然能复燃。 | 依据是_____________。 |
步骤三 | 另取两支试管,各加入5mL过氧化氢溶液,再向试管中分别加入少量二氧化锰粉末和红砖粉末,观察到加入二氧化锰的试管产生气泡的速率明显大于加入红砖粉末的试管。 | _____________。 |
[反思评价]小红对步骤三的结论提出质疑,理由是_____________。
[拓展提升]小军使用另外一种仪器也完成了步骤三的实验,并且得出了同样的结论,他选择的是图中提供的仪器_____________(填字母序号),使用该仪器的优点是_____________(答一点即可),具体的操作是_____________。