题目内容
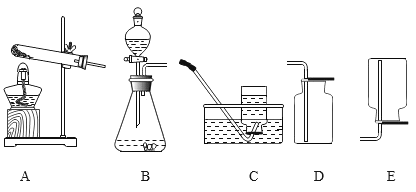
【题目】实验室部分装置如图所示,请回答下列问题。
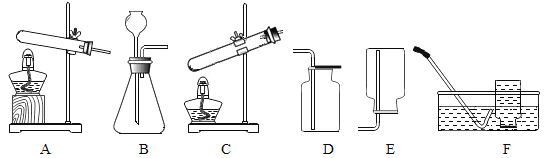
(1)实验室中我们可以通过多种反应原理制取氧气(O2),选择的装置也有所不同,请完成下表。
药品选择 | 反应原理(文字表达式) | 发生装置(填装置标号) | 收集装置(填装置标号) |
过氧化氢(H2O2)溶液、二氧化锰(MnO2) | _______ | _____ | ⑤_____ |
氯酸钾(KClO3)、二氧化锰(MnO2) | ③_____ | ④______ |
(2)选用F装置收集气体时,下列实验操作正确的是____(填序号)。
①反应前,将集气瓶注满水,用玻璃片盖着瓶口,倒立在盛水的水槽中
②开始反应后,等到气泡连续且均匀时,再将导管口移入集气瓶
③收集气体后,将集气瓶盖上玻璃片再移出水槽
(3)在进行“氧气的实验室制取与性质”实验时,若用品中提供棉花,选用高锰酸钾(KMnO4)制取氧气,并将收集到的气体进行铁丝燃烧实验,则制取氧气的发生和收集装置最好选择____(填字母)。
【答案】过氧化氢![]() 水+氧气 B 氯酸钾
水+氧气 B 氯酸钾![]() 氯化钾+氧气 A D或F ①②③ AF
氯化钾+氧气 A D或F ①②③ AF
【解析】
(1)①过氧化氢在二氧化锰作催化剂的条件下反应生成水和氧气,故反应的文字表达式写为:过氧化氢![]() 水+氧气;
水+氧气;
②用过氧化氢溶液与二氧化锰来制取氧气的反应是固体与液体在常温条件下反应生成气体,应选择固液常温发生装置,即装置B,故填B;
③氯酸钾在二氧化锰做催化剂与加热的条件下反应生成氯化钾和氧气,故反应的文字表达式写为:氯酸钾![]() 氯化钾+氧气;
氯化钾+氧气;
④用氯酸钾制取氧气是固体受热反应生成气体,应选择固体受热发生装置,且给固体物质加热时试管口应略向下倾斜,即装置A,故填A;
⑤氧气的密度大于空气的密度,收集氧气可选择向上排空气法,即装置D,氧气不易溶于水,收集氧气还可选择排水法,即装置F,故填D或F。
(2)F装置为排水法收集气体,其操作步骤为:反应前,将集气瓶注满水,用玻璃片盖着瓶口,倒立在盛水的水槽中,开始反应后,等到气泡连续且均匀冒出时,再将导管口移入集气瓶,收集满气体后,将集气瓶盖上玻璃片再移出水槽,故填①②③。
(3)用高锰酸钾制取氧气是固体受热反应生成气体,应选择固体受热发生装置,且给固体物质加热时试管口应略向下倾斜,即装置A,进行铁丝燃烧实验时,盛氧气的集气瓶中应盛有少量的水,所以收集氧气时可选择排水法,即装置F,故填AF。

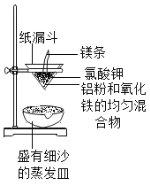
【题目】铝和氧化铁的反应:2A1+Fe2O3![]() Al2O3+2Fe,称为“铝热反应”(如图所示),引燃镁条,漏斗内的物质熔化,镁条燃尽,漏斗下端仍持续产生大量熔融物落入沙中,该熔融物可用于焊接铁轨。
Al2O3+2Fe,称为“铝热反应”(如图所示),引燃镁条,漏斗内的物质熔化,镁条燃尽,漏斗下端仍持续产生大量熔融物落入沙中,该熔融物可用于焊接铁轨。
(1)实验中镁条的作用是_____;氧化铁和铝粉都用粉末状的,原因是_____。
(2)某学习兴趣小组对所得熔融物的成分进行了探究。
(查阅资料)
①金属铝不但能和酸溶液(如稀盐酸)反应产生氢气,还能和强碱溶液(如氢氧化钠溶液)反应产生氢气。
②Al、A12O3、Fe、Fe2O3的熔点、沸点数据如下:
物质 | A1 | Al2O3 | Fe | Fe203 |
熔点/℃ | 660 | 2054 | 1535 | 1462 |
沸点/℃ | 2467 | 2980 | 2750 | - |
(实验猜想)
(3)某同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是:该反应放热能使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金。你认为他的解释是否合理?_____(填“合理”或“不合理”)。
(4)铝与稀盐酸反应的化学方程式为_____。
(5)请你根据已有知识找出一种验证产物中有Fe的最简单的方法:_____。
(实验验证)
(6)设计一个简单的实验方案,证明上述所得的熔融物中含有金属铝,请填写下列表格:
实验步骤 | 实验现象 | 实验结论 |
取少量冷却后的熔融物于试管中,加入_____ | _____ | 熔融物中含有铝 |