题目内容
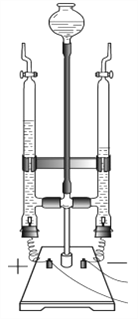
【题目】利用下图装置证明一氧化碳的部分性质并验证产物。

① 氧化铜为_____色粉末,其中氧元素以_______态存在。
② 加热玻璃管后,a中发生反应的化学方程式是________,反应后a中固体的质量_________(选填“变大”“变小”或“不变”)。
③ b中盛放的液体所含的溶质是____________________。
④ c处点燃后,火焰呈________色。
⑤ a中发生的反应证明了一氧化碳具有__________性。
【答案】黑 化合 CO+CuO![]() Cu+CO2 变小 Ca(OH)2(氢氧化钙、熟石灰) 淡蓝 还原性
Cu+CO2 变小 Ca(OH)2(氢氧化钙、熟石灰) 淡蓝 还原性
【解析】
①化合态的氧元素指化合物中有氧元素;
②根据反应物、生成物以及反应条件书写反应方程式;结合质量守恒定律填空;
③b中盛放的液体是用来检验二氧化碳气体的;
④根据CO燃烧的现象进行分析;
⑤玻璃管中发生的反应是一氧化碳与氧化铜反应生成铜和二氧化碳.
解:①氧化铜是黑色粉末,氧化铜中氧元素只有化合态存在.
故填:黑;化合;
②一氧化碳与氧化铜在加热的条件下反应,生成铜和二氧化碳;由于氧化铜被还原成了铜,失去氧元素,故质量减小;
故填:CuO+CO △Cu+CO2;变小;
③一氧化碳与氧化铜在加热的条件下反应,生成铜和二氧化碳,b中盛放的液体是澄清石灰水,用来检验二氧化碳气体的,故该液体所含的溶质是Ca(OH)2(氢氧化钙、熟石灰).
故填:Ca(OH)2(氢氧化钙、熟石灰);
④CO被点燃后,发出淡蓝色火焰;
故填:淡蓝;
⑤一氧化碳与氧化铜反应生成铜和二氧化碳,说明一氧化碳具有还原性.
故填:还原性.

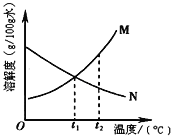
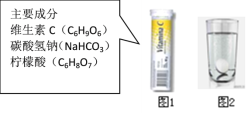
【题目】某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。该小组同学进行如下探究。
探究一:定性探究气体的成分。
(猜想与假设)小华说:该气体可能是CO2、O2、CO、H2、N2。
小明说:不可能含有N2,因为_____________。
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO____________。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
(进行实验)
实验编号 | 实验操作 | 实验现象 |
① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(得出结论)(1)由实验①可知该气体中肯定含_____,写出实验室制取该气体的化学方程式_______。
(2)由实验②___ (填“能”或“不能”)确定该气体中不含氧气,理由是______。
探究二:定量探究。
小明取了一定量该维C泡腾片,放入足量的水中,将产生的气体全部通入足量的澄清石灰水,充分反应后,将瓶中的沉淀过滤出来,称得质量为10g,求生成的二氧化碳气体的质量______。(写出计算过程)
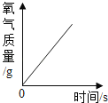
【题目】课外活动小组为了确定某石灰石的成分,取样品25g,分五次加入相同质量、溶质质量分数一定的稀盐酸(杂质不溶于水,也不与稀盐酸反应),部分数据记录及加入盐酸与生成气体的质量关系图如下,请分析计算:
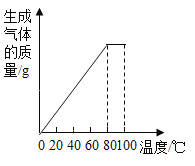
次数 | 第1次 | 第2次 | 第3次 |
加入盐酸的质量/g | 20 | 20 | 20 |
剩余固体的质量/g | 21 | 17 | 13 |
(1)25g样品中碳酸钙完全反应时消耗稀盐酸质量为________g。
(2)25g样品中杂质的质量是________g。
(3)所加稀盐酸的溶质质量分数________。