题目内容
【题目】为除去食盐水中CaCl2、MgCl2、Na2SO4杂质,某化学小组设计了如图方案:试剂1:NaOH,试剂2:BaCl2,试剂3:Na2CO3。
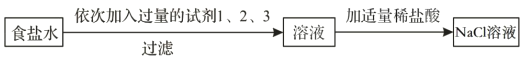
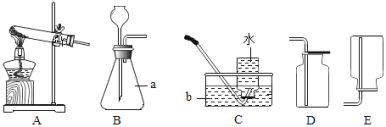
(1)过滤用到的玻璃仪器有烧杯、漏斗和_____。
(2)最后所得溶液中NaCl的质量大于原混合溶液中NaCl的质量,写出一个可使NaCl质量增加的化学方程式_____。
【答案】玻璃棒; BaCl2+Na2SO4═BaSO4↓+2NaCl(合理即可)。
【解析】
(1)过滤用到的玻璃仪器有烧杯、漏斗和玻璃棒。
(2)氯化钡溶液能与硫酸钠溶液反应生成硫酸钡沉淀和氯化钠,氢氧化钠能与氯化镁反应生成氢氧化镁沉淀和氯化钠,碳酸钠与氯化钡溶液反应生成碳酸钡沉淀和氯化钠,碳酸钠能与氯化钙溶液反应生成碳酸钙沉淀和氯化钠,氢氧化钠能与稀盐酸反应生成氯化钠和水,碳酸钠能与稀盐酸反应生成氯化钠、水和二氧化碳。可使精盐中氯化钠质量增加的反应,如![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() (合理即可)。
(合理即可)。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
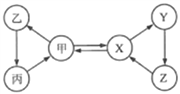
【题目】甲、乙、丙、X、Y、Z六种物质间只通过一步反应就能实现右图中箭头所示的转化。不符合上述要求的一组物质是
选项 | 甲 | X |
A | O2 | H2O |
B | CO2 | CaCO3 |
C | Fe | Fe3O4 |
D | NaOH | NaNO3 |
A. A B. B C. C D. D