题目内容
【题目】为研究酸的化学性质,进行如下实验

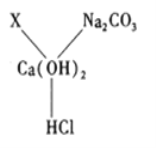
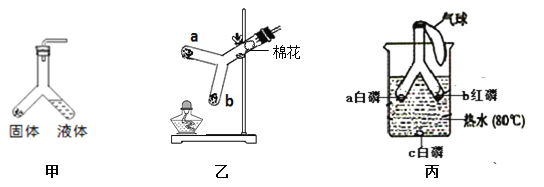
①甲组实验中两支试管均无明显现象,乙组中的现象是:蓝色石蕊试纸变 ,镁带表面有 ,这两组实验说明 .
②丙组实验试管Ⅳ中发生反应的化学方程式是 .
③丙组实验中无明显现象的是 (填试管编号),下列实验不能证明两者发生了反应的是 .
a、测定加入另一反应物前后温度的变化:温度升高
b、测定加入另一反应物前后溶液pH的变化:pH变大
c、先向稀盐酸中滴加酚酞,再逐渐加入另一反应物,一段时间后溶液变红
d、取该试管实验后的剩余溶液滴加碳酸钠,无气泡
④为了验证盐酸具有酸的通性,丙组中还需添加的实验是:向稀盐酸中加入 .
【答案】①变红 有气泡产生 酸的很多反应通常要在水溶液中才能完成
②HCl+AgNO3→AgCl↓+HNO3③Ⅰ b ④活泼金属
【解析】试题分析:①石蕊试液遇酸溶液变红,故乙组中的现象是:蓝色石蕊试纸变变红,金属镁在金属活动性顺序表中排在氢前面,能与酸反应,故镁带表面有有气泡产生;这两组实验不同的实验现象说明:酸的很多反应通常要在水溶液中才能完成
②丙组实验试管Ⅳ中发生反应的化学方程式是:HCl+AgNO3→AgCl↓+HNO3
③丙组实验中无明显现象的是Ⅰ,虽然会发生反应,但是没有现象;a、中和反应放热,故可测定加入另一反应物前后温度的变化:温度升高,可证明两者发生了反应;b、测定加入另一反应物前后溶液pH的变化:pH变大,有可能加入氢氧化钙溶液是将稀盐酸稀释了,溶液的pH也会增大,故此时一定要讲最终pH大于7,错误,c、先向稀盐酸中滴加酚酞,再逐渐加入另一反应物,一段时间后溶液变红,若没有反应,就会立即变化,故可以两者发生了反应;d、根据酸能与碳酸钠溶液反应产生二氧化碳气体,故该试管实验后的剩余溶液滴加碳酸钠,无气泡,证明没有盐酸,故可说明两者发生了反应;故选b
④酸的5个化学性质:1、能与指示剂作用,2、能与活泼金属反应,3、能与金属氧化物反应,4、能与碱发生中和反应,5、能与某些盐反应,故丙组中还需添加的实验是:向稀盐酸中加入活泼金属