题目内容
元素周期表是学习化学的重要工具.下面是元素周期表中1~18号元素原子核外电子排布,我们对它进行研究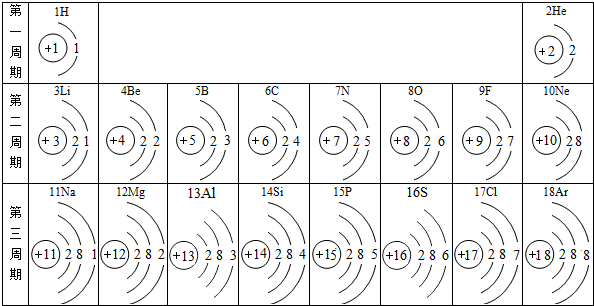
(1)表中磷原子的核电荷数是 ,第三周期中具有相对稳定结构的元素是
在化学反应中,铝原子比较容易 (填“得到”或“失去”)电子变成离子,其离子符号为: 上述元素在周期表中处于同一周期的原因是
(2)在同一族中,各元素的原子结构呈现的规律是 (任写一点);
(3)小明同学所画的某元素的原子结构示意图 ,该元素符号为Br.如图中x= ,上表表示的微粒中,与Br化学性质相似的元素的名称是 .
,该元素符号为Br.如图中x= ,上表表示的微粒中,与Br化学性质相似的元素的名称是 .

(1)表中磷原子的核电荷数是
在化学反应中,铝原子比较容易
(2)在同一族中,各元素的原子结构呈现的规律是
(3)小明同学所画的某元素的原子结构示意图
 ,该元素符号为Br.如图中x=
,该元素符号为Br.如图中x=考点:元素周期表的特点及其应用,原子结构示意图与离子结构示意图
专题:化学用语和质量守恒定律
分析:(1)根据原子结构示意图中,圆圈内数字表示核内质子数;若粒子的最外层电子数为8(氦为2个),属于相对稳定结构;进行分析解答.
若原子的最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子.根据元素周期数与电子层数的关系进行分析解答.
(2)根据在同一族中,电子层数的变化、最外层电子数的特点等,进行分析解答.
(3)当质子数=核外电子数,为原子;元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,据此进行分析解答.
若原子的最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子.根据元素周期数与电子层数的关系进行分析解答.
(2)根据在同一族中,电子层数的变化、最外层电子数的特点等,进行分析解答.
(3)当质子数=核外电子数,为原子;元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,据此进行分析解答.
解答:解:(1)原子结构示意图中,圆圈内数字表示核内质子数(即核电荷数),则表中磷原子的核电荷数是15.
若粒子的最外层电子数为8(氦为2个),属于相对稳定结构,故第三周期中具有相对稳定结构的元素是氩元素.
铝原子的最外层电子数为3,在化学反应中,铝原子比较容易失去3个电子变成离子,其离子符号为Al3+;由元素周期表中某一周期元素的原子结构示意图可以看出,处于同一周期的原子,核外电子层数相同.
(2)在同一族中,从上到下电子层数递增;最外层电子数相等;从上到下核电荷数增大等.
(3)当质子数=核外电子数,为原子,则35=2+8+18+x,x=7;最外层电子数相同的元素化学性质相似,与Br化学性质相似的元素的名称是氟和氯.
故答案为:(1)15;氩;失去;Al3+;核外电子层数相同;(2)从上到下电子层数递增;(3)7;氟和氯.
若粒子的最外层电子数为8(氦为2个),属于相对稳定结构,故第三周期中具有相对稳定结构的元素是氩元素.
铝原子的最外层电子数为3,在化学反应中,铝原子比较容易失去3个电子变成离子,其离子符号为Al3+;由元素周期表中某一周期元素的原子结构示意图可以看出,处于同一周期的原子,核外电子层数相同.
(2)在同一族中,从上到下电子层数递增;最外层电子数相等;从上到下核电荷数增大等.
(3)当质子数=核外电子数,为原子,则35=2+8+18+x,x=7;最外层电子数相同的元素化学性质相似,与Br化学性质相似的元素的名称是氟和氯.
故答案为:(1)15;氩;失去;Al3+;核外电子层数相同;(2)从上到下电子层数递增;(3)7;氟和氯.
点评:本题难度不大,灵活运用元素周期表中元素的信息、原子结构示意图的含义是正确解答本题的关键.

练习册系列答案
相关题目
下列说法正确的是( )
| A、与元素化学性质关系最密切的是它的最外层电子数 |
| B、原子是保持物质化学性质的最小微粒 |
| C、在原子中没有带电荷的微粒 |
| D、原子的质量集中在核外电子上 |