题目内容
【题目】下图为某小组探究金属化学性质的两组实验。
实验I | 实验II |
|
|
①实验I中以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为该实验设计不够合理,理由是______________;
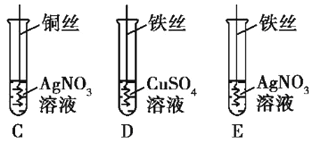
②写出实验II中C试管内反应的化学方程式_____________;
③实验II中要验证Cu、Fe、Ag的金属活动性顺序,至少要做的实验是_____(填字母序号)。
【答案】酸的种类不同 Cu+2AgNO3=2Ag+Cu(NO3)2 CD
【解析】
(1)该实验中没有控制酸的种类相同,冒出气泡的多少可能与酸的种类有关。
(2)铜与硝酸银反应生成硝酸铜和银,反应的方程式为:Cu +2AgNO3=2Ag +Cu(NO3)2。
(3)C实验可以得出铜大于银,D实验可以得出铁大于铜,E实验可以得出铁大于银,由CD就可以推得铁大铜大银,故不需要做E实验,故选CD 。

练习册系列答案
相关题目
【题目】补齐连线。请从A或B两题中任选一个作答,若两题均作答,按A计分。
A 用途—性质 | B 事故—处理方法 | ||
氮气做保护气________ | 升华吸热 | 炒菜时油锅着火________ | 用液态二氧化碳灭火器扑灭 |
石墨用作电极材料________ | 化学性质稳定 | 厨房煤气管道漏气________ | 立即盖上锅盖 |
干冰可用于人工降雨________ | 导电性 | 图书馆内图书着火________ | 立即关闭阀门并开窗通风 |