题目内容
【题目】图一是A、B两种物质的溶解度曲线。![]() ℃时,将等质量的A和B分别加入盛有100g水的两只烧杯中,充分搅拌并恢复至原温度后,现象如图二所示。
℃时,将等质量的A和B分别加入盛有100g水的两只烧杯中,充分搅拌并恢复至原温度后,现象如图二所示。
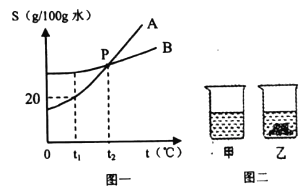
①图中P点的含义_____________。
②![]() ℃时,50克水中最多能溶解A______克。
℃时,50克水中最多能溶解A______克。
③烧杯甲中溶液是否达到饱和状态?________(填“是”、“否”或“无法判断”),其中的溶质是_______(选填“A”或“B”)。
④若A中混有少量B,提纯A采用的方法是_________。
⑤关于图二烧杯内的物质,下列说法正确的是_________。
A. 蒸发一定量的水,两烧杯中都一定有固体析出
B. 烧杯甲中溶液溶质的质量分数大于烧杯乙中溶液溶质的质量分数
C. 将两个烧杯中的溶液混合,充分搅拌后,烧杯中一定还有剩余固体
D. 将温度升高到![]() ℃,两烧杯内溶液中溶质的质量分数一定相等(不考虑水的蒸发)
℃,两烧杯内溶液中溶质的质量分数一定相等(不考虑水的蒸发)
【答案】t2℃时,A、B的溶解度相等 10 无法判断 B 降温结晶 BD
【解析】
①图中P点的含义是:t2℃时,A、B的溶解度相等;
②由溶解度曲线可知,t1℃时A的溶解度为20g,那么50克水中最多能溶解10gA;
③由图二可知,甲烧杯中没有未溶解的晶体,故烧杯甲中溶液是否达到饱和状态无法判断,可能恰好饱和,也可能不饱和;t1℃时,B的溶解度大于A,乙中固体有剩余,甲中没有,说明甲中的溶质是B,故填B;
④由溶解度曲线可知,A、B溶解度都随温度的升高而增大,且A受温度影响变化较大,B受温度影响变化较小,故若A中混有少量B,提纯A采用的方法是:降温结晶;
⑤A、由于烧杯甲中溶液是否达到饱和状态无法判断,故蒸发一定量的水,甲烧杯中可能有固体析出,选项错误;
B、等质量的A和B分别加入盛有100g水的两只烧杯中,甲烧杯中全部溶解,乙烧杯中有部分未溶解的固体,故烧杯甲中溶液溶质的质量分数大于烧杯乙中溶液溶质的质量分数,选项正确;
C、由图可知,乙是A物质的饱和溶液,甲是B物质的溶液,甲中能溶解A物质,但是否能够完全溶解,无法判断,选项错误;
D、由图可知,t2℃时,A、B两物质的溶解度相等,且B的溶解度t2℃时大于t1℃,故将温度升高到t2℃,两烧杯内溶液中溶质的质量分数一定相等(不考虑水的蒸发),选项正确。故选BD。

【题目】在一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如下表所示,下列说法错误的是( )
物 质 | 氧 气 | 二氧化碳 | 水蒸气 | W |
反应前质量/g | 50 | 1 | 1 | 23 |
反应后质量/g | 2 | 45 | 28 | x |
A. 根据质量守恒定律,x的值应为0 B. 反应后的生成物是二氧化碳和水
C. 物质W含碳、氢、氧三种元素 D. 物质W只含碳和氢两种元素
【题目】下列图像能正确反映对应变化关系的是
|
|
|
|
A.向一定质量的AgNO3和Cu(NO3)2的混合溶液中不断加入铁粉 | B.将浓硫酸露置在空气中 | C. 在恒温条件下,将饱和的NaCl溶液蒸发适量水 | D.向一定质量的饱和石灰水中加入生石灰 |
A. A B. B C. C D. D