题目内容
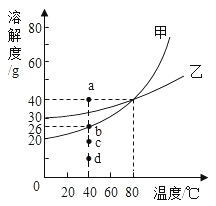
【题目】现有一包含有氯化钠固体的纯碱样品,为测定其成分,同学们取一定质量的这种“纯碱”样品于试管中,加入103g稀盐酸,恰好完全反应,得到4.4g气体。将所得溶液冷却至t℃,恰好成为该温度下的饱和溶液,经测定溶液中的溶质含钠元素的质量为13.8g。求反应后所得溶液中溶质的质量分数。
【答案】26.5%
【解析】
设:碳酸钠的质量为x,生成氯化钠的质量为y。
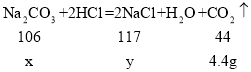
![]() x =10.6g
x =10.6g
![]() y =11.7g
y =11.7g
溶液中的溶质(氯化钠)质量=18.![]()
原固体中NaCl的质量=35.1g-11.7g=23.4g;
所得溶液的质量=23.4g+10.6g+103g-4.4g=132.6g
所得溶液中溶质的质量分数为:![]()
答:反应后所得溶液中溶质的质量分数为26.5%。

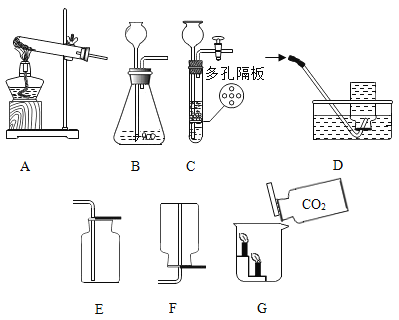
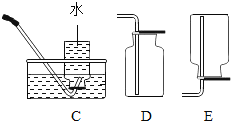
【题目】(1)请结合图示实验装置,回答下列问题。
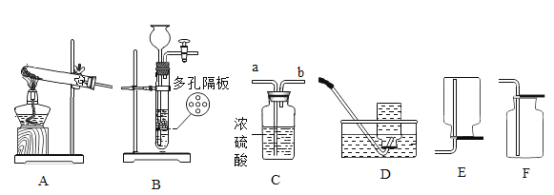
①实验室用高锰酸钾制取氧气,发生装置应选择上述装置中___________(填标号);若用过氧化氢溶液制取干燥的氧气,装置合理的连接顺序为:发生装置→C→___________(填标号);连接装置时,发生装置的出气口应与装置C中_____________(填“a”或“b”)端相连。
②实验室使用B装置制取二氧化碳的突出优点是____________;将制得的二氧化碳通入紫色石蕊试液中,观察到的现象是_____________。
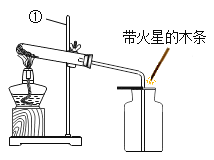
(2)某化学兴趣小组用石灰石和盐酸制取一瓶CO2,验满后,将澄清石灰水倒入集气瓶中,发现没有变浑浊。兴趣小组对这个异常现象进行了探究。
(提出问题)澄清石灰水为什么没有变浑浊?
(查阅资料]①CO2过量时,CaCO3沉淀会转化为可溶于水的Ca(HCO3)2;
②AgCl不溶于稀硝酸
(提出猜想)I.石灰水已完全变质 Ⅱ_______.Ⅲ.CO2中混有HCl
(实验方案)兴趣小组用原药品继续制取CO2,并进行探究。
制备CO2的化学方程式为___________。
实验步骤 | 实验现象 | 实验结论 |
1.取少量澄清石灰水于试管中,加入________溶液。 | 产生白色沉淀 | 猜想I不成立 |
2.将少量气体通入盛有澄清石灰水的试管中 | __________ | 猜想Ⅱ不成立 |
3.____________ | ______________ | 猜想Ⅲ成立 |
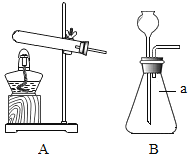
【题目】(1)根据下图的实验装置,回答问题:
发生装置 | 收集装置 | 洗气装置 |
|
|
|
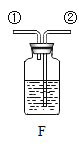
①图B中仪器a的名称_____。
②实验室用加热氯酸钾和二氧化锰混合物制取氧气的化学方程式为:_____,发生和收集装置为_____(填字母)。
③实验室用石灰石和稀盐酸反应制取二氧化碳,其中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置来除去,则混合气体应从F装置的_____端口(填“①”或“②”)通入,F中发生的化学方程式为_____。
(2)为了探究碱的性质,进行如图所示的实验。

①图甲所示,加入一定量的盐酸后,溶液由红色变为了无色,证明了盐酸和NaOH发生了中和反应,且反应后的溶液中一定没有的溶质是_____。张明对甲实验所得溶液的溶质成分产生了兴趣,对反应后溶液变为无色提出了以下两种猜想:
猜想1:溶质成分只有NaCl;
猜想2:溶质成分为_____。
(进行实验)为了验证自己的猜想正确,张明进行了如下实验,请你和他一起完成下列实验报告:
实验操作 | 实验现象 | 实验结论 |
取少量甲实验所得溶液于试管中,并往试管中加入_____ | 观察到_____ | 猜想2正确 |
②如图乙和丙所示,同时将两支充满CO2的相同试管分别倒扣在等体积的水和NaOH溶液中,一段时间后丙中试管内液面高于乙。说明NaOH与CO2发生了反应,该反应的化学方程式为_____。本实验中乙的作用是_____。